|
高中化学知识点讲解《物质的量》试题巩固(2019年最新版)(八)
2020-07-28 05:59:22
【 大 中 小】
|
1、选择题 如果1g水中有m个氢原子,则阿伏加德罗常数为
A.m/9
B.9m
C.2m
D.m/2
|
参考答案:B
本题解析:1g水的物质的量为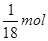 ,氢原子的物质的量为 ,氢原子的物质的量为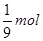 ,又因含有m个氢原子,所以阿伏加德罗常数为9m ,又因含有m个氢原子,所以阿伏加德罗常数为9m
本题难度:一般
2、选择题 配制一定物质的量浓度的NaCl溶液时,主要实验步骤有:
①用适量蒸馏水溶解NaCl固体;
②称量NaCl固体;
③将溶液沿玻璃棒注入到容量瓶中;
④加蒸馏水至溶液的凹液面与容量 瓶的刻度线相切;
⑤计算所需NaCl固体的质量。
正确的操作顺序是
[? ]
A.②①③④⑤
B.⑤②①③④
C.⑤②③①④
D.①②③④⑤
参考答案:B
本题解析:
本题难度:简单
3、选择题 已知32gX与40gY恰好完全反应,生成mgQ和9gH。在相同条件下,16gX和30gY混合充分反应生成0.25molQ和若干物质的量的H,则物质Q的摩尔质量是 (?)
A.63 g・mol─1
B.122 g・mol─1
C.126g・mol─1
D.163 g・mol─1
参考答案:C
本题解析:略
本题难度:简单
4、选择题 300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol・L-1 Ba(OH)2溶液300 mL,反应后溶液中SO42-的物质的量浓度为( )
A.0.4 mol・L-1
B.0.3 mol・L-1
C.0.2 mol・L-1
D.0.1 mol・L-1
参考答案:D
本题解析:n(Al3+)=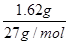 =0.06 mol,则n(SO42-)=0.09 mol,加入的Ba(OH)2溶液中含Ba2+ 0.03 mol,反应后剩余SO42- 0.06 mol,此时溶液的体积为600 mL,因此c(SO42-)=0.1 mol・L-1。 =0.06 mol,则n(SO42-)=0.09 mol,加入的Ba(OH)2溶液中含Ba2+ 0.03 mol,反应后剩余SO42- 0.06 mol,此时溶液的体积为600 mL,因此c(SO42-)=0.1 mol・L-1。
本题难度:一般
5、填空题 实验一:称量9.5g?MgCl2溶于水配成100mL溶液;
实验二:取“实验一”配得的Mg?Cl2溶液25.0mL,稀释到500mL.
(1)“实验一”所得MgCl2溶液的物质的量浓度为______,“实验二”所得Mg?Cl2溶液中Cl-的物质的量浓度为______.
(2)以上两个实验中除了用烧杯、量筒、胶头滴管外,还需要用到的玻璃仪器为______.
(3)配制“实验一”的溶液时,以下几个步骤:①量取;②计算;③溶解;④摇匀;⑤转移;⑥洗涤;⑦定容;⑧冷却.其正确操作顺序为______(填序号).
(4)“实验二”中下列操作可引起所配溶液浓度偏高的有______(填序号).
①洗涤量取MgCl2溶液的量筒,并将洗涤液转移到容量瓶中;
②量取MgCl2溶液时,俯视刻度线;
③转移前,容量瓶中含有少量蒸馏水;
④未洗涤稀释MgCl2溶液时用过的烧杯和玻璃棒;
⑤定容时,俯视刻度线.
参考答案:(1)9.5g?MgCl2 的物质的量n=mM=9.5g95g/mol=0.1mol,配成100mL溶液根据公式C=nV=0.1mol0.1L=1mol/L;实验二:取“实验一”配得的Mg?Cl2溶液25.0mL,稀释到500mL,也就是将原溶液稀释20倍,所以,此时MgCl2的浓度为
1mol/L20=0.05mol/L,所得Mg?Cl2溶液中Cl-的物质的量浓度为MgCl2浓度的两倍,0.1mol/L,
故答案为:1mol/L;0.1mol/L;
(2)配制步骤有计算、称量、溶解、移液、洗涤、定容、摇匀等操作,一般天平称量固体,把氯化镁倒入烧杯进行溶解,冷却后转移到100mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,配成100mL溶液,实验二:取“实验一”配得的Mg?Cl2溶液25.0mL,稀释到500mL,所以需要的仪器有玻璃棒、天平、药匙、烧杯、胶头滴管、100mL容量瓶、500mL容量瓶,所以还需要100mL容量瓶、500mL容量瓶;玻璃棒,
故答案为:100mL容量瓶;500mL容量瓶;玻璃棒;
(3)配制一定物质的量浓度的溶液的基本步骤:计算、量取、溶解、移液、洗涤、定容、摇匀、装瓶存放等操作.据此可得配制“实验一”的溶液正确操作顺序,故答案为:②①③⑧⑤⑥⑦④;
(4)根据公式C=nV计算分析,不当操作对n或V的影响,如果n偏大或V偏小,则所配制溶液浓度偏高.
①洗涤量取MgCl2溶液的量筒,并将洗涤液转移到容量瓶中;量筒在设计时就考虑了不洗涤带来的误差,所以,洗涤量筒只能使配制的浓度偏大,故①正确;
②量取MgCl2溶液时,俯视刻度线;用量筒量取液体时,俯视读数,使所读液体的体积偏小,能使配制的浓度偏小,故②错误;
③转移前,容量瓶中含有少量蒸馏水;容量瓶中有少量水,转移溶液前将容量瓶烘干,对溶质的物质的量、溶液的体积无影响,所以不会造成所配溶液浓度偏高,故③错误;
④未洗涤稀释MgCl2溶液时用过的烧杯和玻璃棒;溶质没有全部转移到容量瓶中,使配制的浓度偏小,故④错误;
⑤定容时,俯视刻度线.定容时俯视容量瓶瓶颈刻度线,会导致溶液的体积偏小,所配制溶液浓度偏高,故⑤正确;故选①⑤;
本题解析:
本题难度:一般
|