1、选择题 在通常状况下呈黄绿色的气体是( )
A.N2
B.H2
C.Cl2
D.CO2
参考答案:N2、H2和CO2都为无色气体,Cl2为黄绿色的气体.
故选:C.
本题解析:
本题难度:一般
2、选择题 下列保存试剂的方法,错误的是(? )
A.氢氟酸要保存在塑料瓶中
B.新制氯水要保存在无色细口瓶中,并放置光亮处
C.液溴要保存在棕色细口瓶中,并在液溴面上加水封
D.单质碘要保存在棕色广口瓶中,并放置阴凉处
参考答案:B
本题解析:药品的保存方法应根据其性质决定:
见光易分解的――避光(棕色瓶);与空气中某些成分反应的或易挥发的――密封(隔绝空气);固体药品――广口瓶;液体药品――细口瓶。
本题难度:简单
3、实验题 (15分)海水蕴含着丰富的资源。在化学实验室里模拟从海水中提取重要的工业原料氯化钠时,设计了以下操作流程:
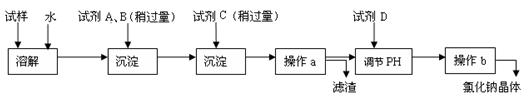
请回答以下问题:
(1)在所提供的试剂中选择:试剂C是?
①Na2CO3?②BaCl2?③稀盐酸
(2)操作b中用到的主要仪器为酒精灯、?、三脚架和玻璃棒。
(3)利用所得的氯化钠制氯气和氢气,并检验氯气的氧化性和测定产生氢气的体积。试按下图所给仪器,设计一套能完成以上实验目的装置,仪器接口的正确连接顺序是:
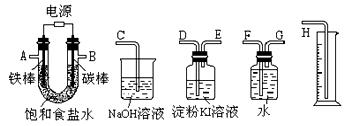
A接?,?接?;B接?,?接?。
(4)写出通入C后,烧杯中所发生的离子反应方程式?
(5)电解氯化钠溶液时的离子方程式为?
若装入的饱和食盐水为75mL,接通电源一段时间,停止通电后,测得氢气为8.4mL(标准状况)。将U形管内的溶液混合均匀,其pH约为_______ 。(假设电解前后溶液体积变化可忽略不计,产生的气体全部逸出)
(6)若想准确读取所得氢气的体积,应采取的操作有?
参考答案:(15分)
(1)(1分)?①?
(2)(1分)?蒸发皿?
(3)(4分)A接? G?,? F?接? H?; B接___D __,___E? _接___ C? _
(4)(2分)?Cl2+ 2OH - ==Cl - +ClO - +H2O
(5)(4分)2Cl - + 2H2O  2OH - + Cl2↑+ H2↑?pH约为12?
2OH - + Cl2↑+ H2↑?pH约为12?
(6)(3分)量筒中液面和广口瓶液面相平;读数时视线与量筒凹液面相平;待整套装置恢复至室温时再行读取数据
本题解析:略
本题难度:简单
4、选择题 19世纪中叶,德国著名化学家李比希曾误将溴认为是氯化碘(ICl)。事实上都是深红棕色液体的氯化碘与溴也极为相似,下列有关它们的结构与性质的比较不正确的是(?)
A.它们的固体都属于分子晶体
B.它们的熔沸点相近
C.等物质的量的ICl和Br2,可氧化等量的SO2
D.它们与水的反应,均为自身氧化还原反应
参考答案:D
本题解析:ICl与水反应的方程式如下:ICl+H2O====HCl+HIO,反应价态没变,故答案为D。
本题难度:简单
5、实验题 (1)向蓝色石蕊试纸上滴加几滴饱和氯水,发现试纸先变红后变白。要确证使石蕊褪色的物质是次氯酸,还必须要做的实验是??:
a.干燥的氯气能否使试纸变白? b.水能否使试纸变白?c.盐酸能否使试纸变白
(2)饱和氯水与石灰石的反应是制取较浓HC1O溶液的方法之一。如图所示在试管中加入过量的块状碳酸钙.再加入约20ml饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去:过滤,将滤?液滴在蓝色石蕊试纸上发现其漂白性比饱和氯水的更强:已知饱和氨水中存在Cl2+H2O H++C1-+HClO.反应后所得的溶液漂白性增强的原因是?(用化学平衡移动原理解释)。
H++C1-+HClO.反应后所得的溶液漂白性增强的原因是?(用化学平衡移动原理解释)。
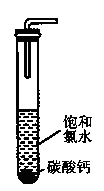
(3)碳酸钙与氯水反应生成的含钙的化合物除氯化钙外,有人提出如下猜想
a.含次氯酸钙? b.含碳酸氢钙? c.含次氯酸钙和碳酸氢钙。
有人认为不可能含有次氯酸钙.他的理由可能是?。
为了证明碳酸氢钙的存在,将滤液分为三份.分别进行以下实验:
①第一份与澄清石灰水混合,立即产生大量白色沉淀:此实验____(填“能”或“不能”)确证溶液中含有碳酸氢钙因为?;
②第二份与稀盐酸混合,立即产生大量无色气体:
③将第三份加热,看到溶液变浑浊且有大量无色气体产生。反应的化学方程式为
④除上述实验外,你能设计的确证碳酸氢钙存在的实验方案是____。
参考答案:(14分,每空2分)
(1)a、c(填abc得1分)
(2)碳酸钙与氢离子反应使其浓度降低,平衡向正反应方向移动,次氯酸浓度增大
(3)次氯酸不能与碳酸钙反应或次氯酸的酸性比碳酸弱
①能,因为Ca(HCO3)2可以与石灰水反应生成白色沉淀
③Ca(HCO3)2 CaCO3↓+CO2↑+H2O
CaCO3↓+CO2↑+H2O
④向滤液中滴加少量稀NaOH溶液,若有白色沉淀生成,证明含有碳酸氢钙。
本题解析:
(1)该实验需要做的是对比实验和空白实验,故答案为a、c
(2)根据平衡移动的原理,增加HClO的浓度,漂白性增强,故可以解释。
(3)根据化合物的性质进行相关的探究,可以得到答案。
本题难度:一般