1�������� PCl5��һ�ְ�ɫ���壬���ȵ�160�治����Һ̬�ξͱ�����������180���µ������ܶ�(�ۺϳɱ�״��)Ϊ9.3g/L, ����Ϊ�㣬P��Cl����Ϊ204pm��211pm���֡��������ȵ�250��ʱ���ѹ��Ϊ����ֵ��������PCl5�ڼ�ѹ����148��Һ�����γ�һ���ܵ�������壬���P��Cl�ļ���Ϊ198pm��206pm���֡�(P��Cl���ԭ������Ϊ31.0��35.5)�ش��������⣺(1)180����PCl5�����д���ʲô���ӣ�Ϊʲô��д������ʽ����������ṹ��(2)��250����PCl5�����д���ʲô���ӣ�Ϊʲô��д������ʽ����������ṹ��(3)PCl5����Ϊʲô�ܵ��磿������ķ�ʽ�������͡�(4) PBr5��̬���ӽṹ��PCl5���ƣ���������Ҳ�ܵ��磬�����ⶨ����ֻ����һ��P-Br������PBr5����Ϊʲô���磿���������ʽ�������͡�
�ο��𰸣�
(1)9.5��22.4="208.3g/mol?" (1��)
PCl5��Է�������31.0+35.5��5="208.5?" ?(1��)
�������ΪPCl5? (1��)
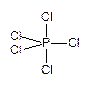
����������������ĸ������ȴ������������⡣����(1)ֻ�漰��һ�仰��������Ϣ�����ۺϳɱ�״̬�������ܶȺ����Ȼ��Ļ�ѧʽ��������������ѧ��ѧ���ݵļļ��㣬�Ϳ��Եó���180���µ�PCl5�ǵ��壬��PCl5�������ķ���ʽ��PCl5������5��Clԭ��Χ����Pԭ�����У���Ϣ�������������ֲ�ͬ������P-Cl�����ɼ���������ƽ�������εķ���(������������һ��)��һ��������ά����ṹ����ά����ṹ�����������֣�����˫�����Ľ��壬���ߵļ��Բ������㣬����PCl5����������˫�ͷ��ӡ�����(2)�������Ϣ�ǵڶ��仰�����ġ�����Ϣ���ɱ�����PCl5�����ڼ��ȵ�250��ʱ�ֽ��ˣ����ɵ���/Ħ����������̬���ӡ����ַֽⷴӦ��������˵���е�ѧ����������Ϥ�ģ���������ͭ�ֽ�����������ͭ���������������̷ֽ��������������̺���������������ֽ����ɶ�������������ȵȡ������ǽ�����֪ʶǨ�Ƶ��Ȼ������������ԣ�������������Ȼ��ķֽ���������Ȼ��������������������Ҳ����Ӱ�����������⣬��������������������������ܵ���ۣ�ҲҪ���ܿ��飬���������ʱ�������������ʿ��飬����Եڶ��ʵ���Ϣ�ṩ�ý��١�����(3)�漰���ǵ���ʵĻ����������ʵĶ���֮һ�����������ܹ����硣������ѧ�α��������ĵ������ӵ����ۺ��١����������ȸ���PCl5�����ܵ������Ϣ���������ϢӦ������������������������Ӵ��ڡ���ô���������������أ��������Ϣ�Ǹ������������ֲ�ͬ��P-Cl����������ų���һ����Cl�C��һ����PCl4+�Ŀ��ܣ���Ϊ����λ��PCl4+������β��������ֲ�ͬ�ļ���(�����������������ͻ���ƽ���ı���)�������������ӿ�����PCl4+��PCl6�C�����С���ڱ����б����˻����ṹʽ֮��������Ϊ���ٰ�ʾ������(4)�Ƕ�����(3)��һ�������Եİ�ʾ����˼����˵�������ȸĻ����壬��PCl6�C���Ƶ�PBr6�C�Dz����γɵģ�������е�������ֻ�������ӡ����ѧ�����и��������ӱ������Ӵ�ö��ͼ�ͻ�����6�������Ӱ��ڰ뾶��С��P5+�������ʵ��̫���ˣ��������ˣ�����С�������������п��ܵġ�ѧ��ѧ����ѧ������Ҫ�и�������������������Ǵ���������ȱ�ٵ�˼ά��ʽ��������ǻ�ѧ����һ������־Ϊ�����������ᷢչ�������ʢ����һ�������˵�Ե��֮һ�������������������������
�����Ѷȣ�һ��
2��ѡ����
A��NCl3����Ϊԭ�Ӿ���
B��������N��Cl���ǷǼ��Թ��ۼ�
C��NCl3��һ�ֺ����Լ��ļ��Է���
D��N��Cl���ܴ�NCl3�е��
�ο��𰸣�C
���������A.����NCl3�ڳ����³�Һ̬�������и�������ӳ������Σ����ԣ����γɵľ���Ϊ���Ӿ��壻
B.ֻ��ͬ�ַǽ���Ԫ�ؼ�����γɷǼ��Լ�����ͬ�ַǽ���Ԫ�ؼ�Ĺ��ۼ�һ��Ϊ���Թ��ۼ�������N��Cl����Ϊ���Լ���
C.����NCl3���ӳ������Σ�����NH3���ӣ���Ϊ���Է��ӡ�C��ȷ��
D.����NCl3�ڳ����³�Һ̬�������е㲻�ߡ�
�����Ѷȣ�һ��
3��ѡ���� ��H2��Cl2��ɵĻ�����徭���ճ�ַ�Ӧ��ͨ��1000mL0.1 mol/L��NaOH��Һ��,ͼ�ױ�ʾij�����ӵ����ʵ�����ͨ�����������仯���ߡ���n=0.02molʱ������ǰ�Ļ��������H2��Cl2?�����ʵ�����֮��Ϊ?��?��
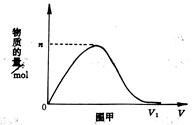
A��4��3
B��7��3
C��3��5
D��3��7
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
4��ѡ���� ��1897��Ӣ���״�ʹ�������Ը�ˮ��������������������������ˮ�����Ѿ�������100�������ʷ��Ŀǰ���ҹ������������Ȼ��������������������ˮ���о���������������֮���Գ�����������ˮ������ԭ����
A�������ж������Զ���ϸ��������
B���������д̼�����ζ������Ѭ��ϸ��������
C��������ˮ��Ӧ���ɾ���ǿ�����Ե�HClO������ɱ��ϸ��������
D��������������ˮ�����Ĺ��ռ����죬���ڲ������ҳɱ���
�ο��𰸣�CD
���������������ˮ��Ӧ���ɾ���ǿ�����Ե�HClO������ɱ��ϸ��������������������������ˮ�����Ĺ��ռ����죬���ڲ������ҳɱ��ͣ���ѡCD��
�����������ǻ���������Ŀ��飬������������ʵ�ʣ��ѶȲ���ס���ɡ������ڵ���ѧ����ѧϰ��Ȥ��ѧϰ�����ԣ�����ѧ������֪����
�����Ѷȣ���
5��ѡ���� ���й�����ˮ����������ȷ���ǣ�������
A��������ˮ��ֻ��Cl2��H2O����
B��������ˮ��ʹ��ɫʯ����ֽ�ȱ�����ɫ
C����ˮ��������ɫ��ϸ���Լ�ƿ��
D����ˮ���������������ǿ
�ο��𰸣�A����ˮ�к���HClO��Cl2��H2O�ȷ��ӣ���A����
B��������ˮ����HCl����ʹ��ɫʯ����ֽ�ȱ�죬����HClO����ʹ��ɫʯ����ֽ��ɫ����B��ȷ��
C������HClO�����ֽ⣬��Ӧ��������ɫ�Լ�ƿ�У���C����
D��HClOΪ���ᣬHClO�����ֽ⣬����HCl����Һ������ǿ����D��ȷ��
��ѡBD��
���������
�����Ѷȣ�һ��