| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《键参数――键能、键长与键角》高频考点特训(2019年练习版)(十)
(5)CuCl的晶胞结构如右图所示,其中Cl-的配位数(即与Cl-最近距离的Cu+的个数)为?。 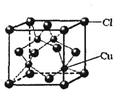 参考答案:(1)3d9(1分);O>N>H(1分)?(2)V型(1分); 本题解析:(1)根据构造原理可知,铜离子的基态外围电子排布式为3d9。非金属性越强,电负性越大,即电负性大小顺序是O>N>H。 本题难度:一般 4、选择题 下列关于物质说法正确的是 参考答案:B 本题解析: 本题难度:简单 5、选择题 下列说法正确的是 参考答案:D 本题解析:A.四者均为水分子,只不过原子核内的中子数略有不同,而同素异形体是指同种元素的不同单质,错误 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《化学平衡》.. | |