1������� ��1��Ũ�Ⱦ�Ϊ0.1mol/L��8����Һ����HNO3?��H2SO4?��CH3COOH?��Ba��OH��2?��NaOH?��CH3COONa?��KCl?��NH4Cl����ҺpHֵ��С�����˳���ǣ�����д��ţ�______��
��2���Ȼ���ˮ��Һ��______�ԣ�ԭ���ǣ������ӷ���ʽ��ʾ����______����AlCl3��Һ���ɣ����գ����õ�����Ҫ���������______��
��3���ڢ�pH=3��������Һ�͢�pH=3�Ĵ�����Һ�У��ֱ�Ͷ������п�ۣ���ʼʱ��Ӧ���ʴ�СΪ��______�ڣ�����=������������ͬ������Ӧ���������ɵ�H2�������ͬ��ͬѹ����______�ڣ�����ˮϡ����ͬ�ı�����pHֵ��______�ڣ�
�ο��𰸣���1����Һ�ʼ��Ե��У��ܢݢޣ����Т�Ϊ��Ԫǿ���ΪһԪǿ���ˮ��ʼ��ԣ�Ũ����ͬʱ��PH���ܣ��ݣ��ޣ�
��Һ�����Ե��У��ߣ�
��Һ�����Ե��У��٢ڢۢ࣬���Т�ΪһԪǿ�ᣬ��Ϊ��Ԫǿ�ᣬ��Ϊ���ᣬ��ˮ������ԣ�Ũ����ͬʱ��
PH���ڣ��٣��ۣ��࣬
�ʴ�Ϊ���ڢ٢ۢ�ߢޢݢܣ�
��2���Ȼ���Ϊǿ�������Σ�Al3+��ˮAl3++3H2O
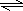
Al��OH��3+3H+����Һ�����ԣ�
�Ȼ�����ˮ��Ϊ���ȹ��̣����ȴٽ�ˮ�⣬��AlCl3��Һ���ɣ��õ�Al��OH��3�����գ��ֽ�����Al2O3�����õ�����Ҫ���������Al2O3��
�ʴ�Ϊ���Al3++3H2O
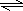
Al��OH��3+3H+��Al2O3��
��3������Ϊ���ᣬpH=3��������Һ��pH=3�Ĵ�����Һ��Ƚϣ�����Ũ�ȴֱ�Ͷ������п�ۣ���ʼʱ������Һ��Ӧ���ʴ���������ʵ����࣬����ȫ��Ӧ���������࣬��ˮϡ��ʱ�������һ�����룬��ˮϡ����ͬ�ı���������PH�仯��Χ��
�ʴ�Ϊ��=����������
���������
�����Ѷȣ�һ��
2��ѡ���� ���е��뷽��ʽ��д����ȷ����
A��2H2O H3O++OH��
H3O++OH��
B��H2S H+ + HS��
H+ + HS��
C��NaHS Na++HS��
Na++HS��
D��NaHCO3 = Na+ + HCO3��
�ο��𰸣�C
���������NaHS��ǿ����ʣ����뷽��ʽΪNaHS�� Na++HS����ѡ��C����ȷ���������ȷ�ģ���˴�ѡC��
�����Ѷȣ�һ��
3������� �������ʣ���1��Na����2��Br2����3��Na2O����4��N2O5����5��CO2����6��SO3����7��NH3����8��H2S����9��HCl����10��H2SO4����11��Ba��OH��2���壻��12��NaCl���壻��13�����ǣ���14��NaCl��Һ�����ڵ���ʵ���______�����ڷǵ���ʵ���______���ܵ������______��
�ο��𰸣���ˮ��Һ�л��ۻ�״̬���ܵ���Ļ��������ڵ���ʣ�����������ﵽ�У���3��Na2O����8��H2S����9��HCl����10��H2SO4����11��Ba��OH��2���壻��12��NaCl���壻
�ǵ������ˮ��Һ�к��ۻ�״̬�¶����ܵ���Ļ���������������У���4��N2O5����5��CO2����6��SO3����7��NH3����13�����ǣ�
���������ƶ����ӣ��ܹ�����������У���1��Na����14��NaCl��Һ��
�ʴ�Ϊ����3����8����9����10����11����12������4����5����6����7����13������1����14����
���������
�����Ѷȣ�һ��
4��ѡ���� ���й��ڵ������Һ��������ȷ���ǣ�������
A�������£���pH=7�Ĵ����ƺʹ�������Һ�У�c��CH3COO-����c��Na+��
B��ϡ�ʹ�����Һ����Һ���������ӵ�Ũ�Ⱦ�����
C����pH=5���Ȼ��ƺ�ϡ����Ļ����Һ�У�c��Na+��=c��Cl-��
D��0.1mol?L-1��������Һ�У�c��OH-��=c��H+��+c��HS-��+c��H2S��
�ο��𰸣�A�������£���pH=7�Ĵ����ƺʹ�������Һ��c��H+��=c��OH-��������غ�ʽΪc��H+��+c��Na+��=c��OH-��+c��CH3COO-������c��CH3COO-��=c��Na+������A����
B��ϡ�ʹ�����Һ��c��H+����С��Kw���䣬�����ϡ��ʱc��OH-������B����
C��pH=5����Һ��c��H+����c��OH-�����ɵ���غ��֪��c��Na+��+c��H+��=c��OH-��+c��Cl-��+c��NO3-������c��Na+����c��Cl-��+c��NO3-�����������ӡ������Ӿ���Դ�Ȼ��Ƶĵ��룬��c��Na+��=c��Cl-������C��ȷ��
D��������Һ�У��ɵ���غ��֪c��Na+��+c��H+��=2c��S2-��+c��HS-��+c��OH-�����������غ��֪12c��Na+��=c��S2-��+c��HS-��+c��H2S������c��OH-��=c��H+��+c��HS-��+2c��H2S������D����
��ѡC��
���������
�����Ѷȣ���
5������� ��֪ij��Һ��ֻ����OH-��H+��NH4+��Cl-�������ӣ�ijͬѧ�Ʋ�������Ũ�ȴ�С˳��������������ֹ�ϵ��
��c��Cl-����c��NH4+����c��H+����c��OH-��?��c��NH4+����c��OH-����c��Cl-����c��H+��
��c��NH4+����c��Cl-����c��OH-����c��H+��?��c��Cl-����c��H+����c��NH4+����c��OH-��
��д���пհף�
��1������Һ��ֻ�ܽ�һ�����ʣ����������______��������������Ũ�ȵĴ�С˳��Ϊ������ţ�______��
��2�����������ӵĹ�ϵ���Ϣۣ�������Ϊ______��
���������ӵĹ�ϵ���Ϣܣ�������Ϊ______��
��3����pH��ͬ��NH4Cl��Һ��HCl��Һϡ����ͬ�ı�����������ͼ1��ȷ���ǣ���ͼ����ţ�______��

��4��������Һ���������ȵ�ϡ����Ͱ�ˮ��϶��ɣ���ǡ�ó����ԣ�����ǰc��HCl��______c��NH3?H2O��������ڡ�����С�ڡ����ڡ�����ͬ�������ǰ����c��H+���ͼ���c��OH-���Ĺ�ϵΪc��H+��______c��OH-����
��5����ͼ2��ʾ���ձ���ʢ�ŵ���ҺΪ���ᣬ��ͨ������G��ָ�뷢��ƫת����������______��������Ӧʽ��______��
�ο��𰸣���1�����κ�ˮ��Һ�ж���OH-��H+��������ֻ��һ����ΪNH4Cl��笠�����ˮ�ⷽ��ʽΪNH4++H2O?NH3��H2O+H+����c��Cl-����c��NH4+����ˮ�������ԣ���c��H+����c��OH-������ˮ��ij̶Ⱥ�������c��Cl-����c��NH4+����c��H+����c��OH-�������ٷ��ϣ�
�ʴ�Ϊ��NH4Cl���٣�
��2���������ӵĹ�ϵ��֪��Һ�Լ��ԣ���c��NH4+����c��Cl-��������ҺΪ�Ȼ�狀Ͱ�ˮ�Ļ����Һ��
������ΪNH4Cl��NH3��H2O�����е����ӹ�ϵ��֪��Һ�����ԣ���c��Cl-����c��H+����c��NH4+��������ҺΪ�������Ȼ�淋Ļ����Һ��������ΪHCl��NH4Cl��
�ʴ�Ϊ��NH4Cl��NH3?H2O��NH4Cl��HCl��
��3��pH��ͬ��NH4Cl��Һ��HCl��Һϡ��ʱ�����ӵ�Ũ�ȶ���С����pH���������Ϊǿ����ʣ���pH�仯�̶ȴ��Ȼ��ˮ�������ԣ�ϡ�ʹٽ�ˮ�⣬������Ũ�ȼ�С�ı���С��������������Ũ�ȵı仯����pH�仯С��ֻ��B�������⣬
�ʴ�Ϊ��B��
��4���������Ũ����ͬ��ϡ����Ͱ�ˮ��ϣ���Һ�е�����Ϊ�Ȼ�泥���Һ�����ԣ�������Һǡ�ó����ԣ���ӦΪ��ˮ���Ȼ�淋Ļ����Һ����c��HCl����c��NH3?H2O����
��HClΪǿ����ʣ���ȫ���룬NH3��H2OΪ������ʣ�����ȫ���룬����ǰ����c��H+���ͼ���c��OH-���Ĺ�ϵΪc��H+����c��OH-����
�ʴ�Ϊ��С�ڣ����ڣ�
��5����ͼ2��֪��Zn��Cu���ã�Zn����������Zn+2HCl�TZnCl2+H2������������ӦΪ2H++2e-=H2����
�ʴ�Ϊ��Zn��2H++2e-=H2����
���������
�����Ѷȣ�һ��