1��ѡ���� ���������£��� װ����������ܱ������У�����Ӧ
װ����������ܱ������У�����Ӧ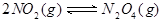 �ﵽƽ�������ѹ��������������ȷ����
�ﵽƽ�������ѹ��������������ȷ����
A��������룬��ѹǿΪԭ��������
B��ƽ�������ƶ�������������ɫһ�����dz
C��������룬ѹǿ����С��ԭ����2��
D��ƽ�������ƶ�����������ܶȲ���
�ο��𰸣�C
���������A����������룬���˲��ѹǿΪԭ����������������ѹǿ��ƽ�������������С�ķ����ƶ�������ƽ�⽫������Ӧ�����ƶ���ѹǿ�������Ļ����Ͻ����С��
B����ƽ�������ƶ�����������ɫ��һ�����dz��������N2O4��Ũ�ȣ�ƽ�������ƶ�����N2O4��Ũ������
C����ȷ��D����ƽ�������ƶ������������ʵ�����С������������������䣬�������������ܶȻ�����
�����Ѷȣ�һ��
2������� �ס��������������ݻ��̶����ҵ��ݻ��ɱ䡣��һ���¶��£������ͨ��3mol N2��4mol H2����Ӧ�ﵽƽ��ʱ������NH3�����ʵ���Ϊamol��
��1����ͬ�¶��£�������ͨ��2molNH3���ұ����ݻ������ͬ������Ӧ�ﵽƽ��ʱ�������ʵ�Ũ�����ƽ������ͬ����ʼʱ���л�ͨ����____mol N2��____mol H2��
��2����ͬ�¶��£���������ͨ��6mol N2��8mol H2���ұ���ѹǿ�����ȣ�����Ӧ�ﵽƽ��ʱ�����ɰ������ʵ���Ϊb mol����a��b______1��2����������ݻ�ʼ����ȣ��ﵽƽ��ʱ�����ɰ������ʵ���Ϊc mol����a��c_____1��2? (�����������������)��
�ο��𰸣���1��2mol N2��1mol H2?��2����?��
�����������1������Ӧ�ﵽƽ��ʱ�������ʵ�Ũ�����ƽ������ͬ��˵��ƽ���ǵ�Ч�ġ�����2mol�����൱����3mol������1mol���������Ҫʹƽ���Ч������Ҫ2mol N2��1mol H2��
��2������ѹǿ�����ȣ�˵��ƽ���ǵ��µ�ѹ�µĵ�Чƽ�⣬���ƽ��ʱƽ�ⰱ�����ʵ������ʵ���b��2a������a��b��1��2�����ڰ��ĺϳ���ѹǿ��С�Ŀ��淴Ӧ�������ܱ���ѹǿ���䣬�������з�Ӧ���ת���ʴ�ƽ��ʱ�������ʵ������ʵ���c��2a����a��c��1��2��
�����Ѷȣ�һ��
3��ѡ���� ��һ������Ag2SO4���������ݻ�����������У���ij�¶��·������з�Ӧ��
Ag2SO4(s) Ag2O(s)��SO3(g)��2SO3(g)
Ag2O(s)��SO3(g)��2SO3(g) 2SO2(g)��O2(g)����ʮ���Ӻ�Ӧ�ﵽƽ�⣬��ʱC(SO3)��0.4 mol/L��C(SO2)��0.1 mol/L����������������ȷ����
2SO2(g)��O2(g)����ʮ���Ӻ�Ӧ�ﵽƽ�⣬��ʱC(SO3)��0.4 mol/L��C(SO2)��0.1 mol/L����������������ȷ����
A��SO3�ķֽ���Ϊ20%
B��ƽ��ʱ��v(O2)��0.005 mol/(L��min)
C��������������ܶ�Ϊ40g/L
D����ѹ�������ڹ�����������
�ο��𰸣�D
��������������������ݻ�Ϊ1L�������ڵ�SO2��SO3�Եķֽ⣬���ݷ���ʽ��֪Ҫ����SO2��0.1 mol����Ҫ�����ֽ��SO3��0.1 mol��ƽ��ʱ�����ڵ�SO3��0.4mol,�����������ֽ����ɵ�SO3�ܹ���0.1+0.4="0.5mol," SO3�ķֽ���Ϊ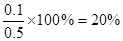 ,A��ȷ����ѡ��ƽ��ʱ
,A��ȷ����ѡ��ƽ��ʱ ��������֮�ȵ��ڼ�����֮�ȿ��Եõ�v(O2)=
��������֮�ȵ��ڼ�����֮�ȿ��Եõ�v(O2)= 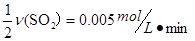 ��B��ȷ����ѡ�����ݷ���ʽ��֪��Ӧ���ɵ����������ʵ���Ϊ0.1mol,������������ܶ�Ϊ
��B��ȷ����ѡ�����ݷ���ʽ��֪��Ӧ���ɵ����������ʵ���Ϊ0.1mol,������������ܶ�Ϊ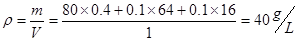 ,����ѹǿ��������ѧƽ����������ƶ�����һ��ƽ�������ƶ����ᵼ�¹����������������������С������D����ѡD.
,����ѹǿ��������ѧƽ����������ƶ�����һ��ƽ�������ƶ����ᵼ�¹����������������������С������D����ѡD.
�����Ѷȣ�һ��
4������� ��12�֣�����β���ﺬ��NO������������ȼ��ȼ�յĸ�����������������Ӧ���£�N2(g) + O2(g)  ?2NO(g)? ��H > 0��֪�÷�Ӧ��2404��ʱ��ƽ�ⳣ��K=64��10-4����ش�
?2NO(g)? ��H > 0��֪�÷�Ӧ��2404��ʱ��ƽ�ⳣ��K=64��10-4����ش�
��1��ij�¶��£���2L���ܱ������г���N2��O2��1mol,5���Ӻ�O2�����ʵ���Ϊ0.5 mol����N2�ķ�Ӧ����?��
��2���ٶ��÷�Ӧ���ں��������½��У��жϸ÷�Ӧ�ﵽƽ��ı�־?��
A������1molN2ͬʱ����1molO2
B����������ܶȲ���
C���������ƽ����Է�����������
D��2V(N2)��=V(NO)��
