1、选择题 下列叙述中,错误的是(?)
A.原子半径:Na>Mg>O
B.13C和14C属于同位素
C.0族元素是同周期中非金属性最强的元素
D.N和P属于第ⅤA族元素,HNO3酸性比H3PO4的强
参考答案:C
本题解析:同周期元素自左向右原子半径逐渐减小,A正确。.13C和14C的质子数相同,质量数不同,所以这两种核素互称为同位素,B正确。同周期非金属性最强的元素位于第ⅦA,C是错误的。同主族元素自上而下非金属性是减弱的,非金属性越强,相应最高价氧化物对应水化物的酸性就越强,D正确。答案选C。
本题难度:简单
2、填空题 (5分)根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:
(1)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式?▲?;
(2)Be(OH)2与Mg(OH)2可用__▲___试剂鉴别,其反应离子方程式为?▲?。
(3)Li和Mg根据对角线规则,性质也相似,则Li在空气中燃烧,主要产物的化学式是__▲____;同时还有少量??▲?生成。
参考答案:各1分?共5分?

本题解析:略
本题难度:一般
3、选择题 稀土是工业味精,邓小平说过“中东有石油,我们有稀土”。稀土元素铈(Ce)主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是(?)
A.已知Ce原子序数是58,则其为镧系元素
B.铈有四种稳定的核素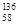 Ce、
Ce、 Ce、
Ce、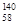 Ce、
Ce、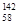 Ce,它们互为同位素
Ce,它们互为同位素
C.用Ce(SO4)2溶液可与硫酸亚铁溶液反应,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+
D.铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑
参考答案:AB
本题解析:A.镧系元素是第57号元素镧到71号元素镥15种元素的统称;B.质子数相同而中子数不同的一类原子互称为镧系元素;C.电荷不守恒;D.由可Fe3+氧化I-可知,Ce4+也可氧化I-,故CeI4不存在,应为CeI3.
本题难度:一般
4、选择题 国外科学家曾将铅(Pb)和氪(Kr)两种元素的原子核对撞,获得了一种质子数为118、
质量数为293的新元素,该元素原子核内的中子数和核外电子数之差为
A.47
B.57
C.61
D.175
参考答案:B
本题解析:对于原子来说,核内的质子数等于核外的电子数。质子数为118,则核外电子数也是118,所以中子数为293-118;该元素原子核内的中子数和核外电子数之差为293-118-118=57。因此选项为B。
本题难度:简单
5、选择题 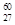 Co是r射线的放射源,关于
Co是r射线的放射源,关于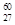 27Co的说法正确的是?
27Co的说法正确的是?
A.质子数为 33
B.中子数为27
C.质量数为60
D.核电荷数为60
参考答案:C
本题解析:在原子结构中,质量数(60)=质子数(27)+中子数,中子数为33,A、B错误;又核电荷数=质子数,D错误。
本题难度:简单