1、选择题 2A+B==3C+4D反应中,表示该反应速率最快的是
[? ]
A. υ(A)= 0.5mol/L・s
B. υ(B)= 0.4mol/L・s
C. υ(C)= 0.8mol/L・s
D. υ(D)= 1mol/L・s
参考答案:B
本题解析:
本题难度:简单
2、选择题 一定条件下,可逆反应N2 +3H2 2NH3?
2NH3?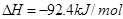 ,有关该反应的叙述正确的是(?)
,有关该反应的叙述正确的是(?)
A.正催化剂能加快正反应速率v正,不影响v逆,所以缩短了反应达平衡所需的时间
B.将lmol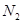 和3mol
和3mol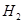 充分反应达到平衡时,放出的热量等于92.4kJ
充分反应达到平衡时,放出的热量等于92.4kJ
C.当c(N2):c(H2):c(NH3)=1:3:2时,反应就达到平衡状态
D.平衡时增大氮气的浓度,达新平衡时N2 转换率减小,H2转化率增大
参考答案:D
本题解析:A、催化剂降低活化能,以相同的倍数增大正逆反应速率;
B、可逆反应不可能进行到底,放出的热量小于92.4KJ;
C、平衡状态浓度之间没有关系,各物质浓度保持不变。
本题难度:一般
3、选择题 在A(g)+ pB(g) qC(g)的反应中,经t秒后C的浓度增加m mol/L,则用B浓度的变化来表示的反应速率是
qC(g)的反应中,经t秒后C的浓度增加m mol/L,则用B浓度的变化来表示的反应速率是
[? ]
A.pq/mt mol・L-1・s-1
B.mt/pq mol・L-1・s-1
C.pm/qt mol・L-1・s-1
D.pt/mq mol・L-1・s-1
参考答案:C
本题解析:
本题难度:简单
4、选择题 .可逆反应达到平衡的根本原因是(?)
A反应混合物中各组分的浓度相等? B.正逆反应都还在继续进行
C.正逆反应的速率均为零? D.正逆反应的速率相等
参考答案:D
本题解析:可逆反应达到平衡的根本原因是正逆反应的速率相等,且不为0,所以选项D正确,答案选D。
本题难度:简单
5、计算题 某温度下N2O4和NO2之间建立起如下的平衡N2O4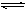 2NO2,测得平衡混合物对空气的相对密度为2.644,求N2O4的分解率。
2NO2,测得平衡混合物对空气的相对密度为2.644,求N2O4的分解率。
参考答案:N2O4的分解率为20%。
本题解析:设N2O4的起始物质的量为1
转化了的N2O4物质的量为x
?N2O4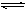 2NO2
2NO2
起始物质的量?1?0
转化物质的量?x?2x
平衡物质的量?1-x?2x
平衡时混合气体的总物质的量为
n总=1-x+2x=1+x
∵ =29・D=29×2.644=76.68
=29・D=29×2.644=76.68
已知N2O4和NO2的相对分子质量分别为92,46,则有:
76.68=(92×(1-x)+46×2x/1+x)
解得x=0.2mol
∴N2O4的分解率为:(0.2/1)×100%=20%
本题难度:简单