1、选择题 盛满等体积NO和NO2的混合气体的试管,倒置在水槽中,反应完毕后液面上升的高度是试管的
A.1/2
B.1/3
C.2/3
D.5/6
参考答案:B
本题解析:略
本题难度:一般
2、计算题 在硝酸生产过程所排放出来的废气中含有NO和NO2,它们污染环境,现用氨催化还原法将它们转化为无毒气体(填名称)____直接排入空气中,写出有关反应方程式:__? __,假设NO和NO2物质的量之比恰好为1∶1,则两者的混合物相当于一种酸酐,写出由烧碱溶液吸收这种酸酐的化学方程式:___? _。
参考答案:N2,6NO2+8NH3 7N2+12H2O
7N2+12H2O
6NO+4NH3 5N2+6H2O
5N2+6H2O
NO+NO2+2NaOH==2NaNO2+H2O
或? N2O3+2NaOH==2NaNO2+H2O
本题解析:正价的氮的化合物与负价的氮的化合物往往可以发生反应生成单质N2。所以NO2与NH3在催化剂作用下生成无毒的N2单质。
NO和NO2物质的量之比为1∶1的混合物,相当于亚硝酸酸酐N2O3,其中N的化合价为+3,与NaOH溶液反应,生成相应的价态的盐和水。
本题难度:一般
3、填空题 测定铜合金中铜的含量,可以用稀硝酸来溶解样品,也可以用双氧水和稀盐酸溶解样品,其反应的化学方程式为: 。假设样品中其他成分不与稀硝酸、双氧水和盐酸反应。
。假设样品中其他成分不与稀硝酸、双氧水和盐酸反应。
①写出铜与稀硝酸反应的离子方程式并标出电子转移的方向和数目____________________。
②在铜与双氧水、盐酸的反应中氧化剂是______________________________,若有2 mol的H2O2参加反应,则电子转移的物质的量是_______________。
③用双氧水和稀盐酸溶解样品与用稀硝酸溶解样品相比较,哪种更好?为什么?____________________。
④若称取样品的质量为a g,用足量的双氧水溶解后,剩余残渣经过洗涤干燥称得质量是b g,
则样品中含铜的质量分数为__________。
参考答案:(1)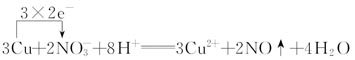 (2)双氧水,4 mol
(2)双氧水,4 mol
(3)双氧水更好,因为双氧水在酸性条件下氧化单质铜后的产物中没有污染空气的有害气体?(4)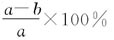
本题解析:①硝酸具有强氧化性,作氧化剂,能把铜氧化生成硝酸铜,而硝酸的还原产物是NO。
②根据方程式可知,双氧水中的氧原子化合价从-1价降低到-2价,因此双氧水作氧化剂。每消耗1mol双氧水,就转移2mol电子。消耗2mol,则转移4mol电子。
③根据反应中的还原产物可判断,双氧水的还原产物是水,没有污染。而硝酸的还原产物是NO,有毒属于大气污染物。
④根据方程式可知,固体中只有铜被溶解,所以固体减少的质量就是混合物中铜的质量,因此铜的质量分数为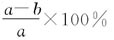 。
。
本题难度:一般
4、选择题 在盛有浓氨水的瓶口上方,悬一沾有下列物质的棉球,有白烟产生的是(?)
A.浓盐酸
B.浓氢氧化钠溶液
C.浓硫酸
D.浓盐水
参考答案:A
本题解析:
正确答案:A
A、HCl+NH3=NH4Cl生成物是白色固体。B和D均不反应;C、反应但无明显现象。
本题难度:简单
5、选择题 将(NH4)2CO3加热到全部转化为气体后,将气体先通过过氧化钠,固体质量增加x g,再通过浓硫酸,液体质量增加y g;若先通过浓硫酸,液体质量增加z g,再通过过氧化钠,固体质量增加w g。则x、y、z、w由大到小的排列顺序是
A.z>y>x>w
B.w>z>y>x
C.y>z>w>x
D.x>y>z>w
参考答案:A
本题解析:
本题化学反应:(NH4)2CO3=2NH3+H2O+CO2
2Na2O2+2H2O=4NaOH+O2
2Na2O2+2CO2=2Na2CO3+O2
2NH3+H2SO4=(NH4)2SO4
设取1mol(NH4)2CO3,分解产生2molNH3、1molH2O、1molCO2
2Na2O2+2H2O=4NaOH+O2? △m
1mol? 2g
2Na2O2+2CO2=2Na2CO3+O2?△m
1mol? 28g
将气体先通过过氧化钠,固体质量增加x g,
X=2g+28g=30g
2NH3+H2SO4=(NH4)2SO4?△m
2mol? 34g
再通过浓硫酸,液体质量增加y g
Y=34g
若先通过浓硫酸,液体质量增加z=2mol×17g/mol+1mol×18g・mol-1=52 g,
再通过过氧化钠,固体质量增加w="28" g。
选A.
本题难度:简单