1、选择题 下列有关说法正确的是()
A.电子层结构相同的微粒其化学性质一定相同
B.元素的原子失去电子数越多该元素还原性就越强
C.同种元索形成的双原子分子中一定含有非极性共价键
D.单质中一定含有化学键
参考答案:C
本题解析:A错误,Na+和F-以及Ne原子的电子层结构相同,但化学性质不相同。
B错误,还原性强弱与失去电子数目没有直接关系。
C正确。
D错误,惰性气体这样的单原子分子不含有任何化学键。
本题难度:简单
2、选择题 零族元素难以形成化合物的本质原因是
A.它们都是惰性元素
B.它们的化学性质不活泼
C.它们都以单原子分子形式存在
D.它们的原子的电子层结构均为稳定结构
参考答案:D
本题解析:零族元素难以形成化合物的本质原因是最外层都已达到稳定结构,不容易和其它原子化合,故选D。
本题难度:一般
3、选择题 短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是 ?(?)?

A.Z 是活泼的金属元素
B.Y的最高价氧化物的水化物是一种强酸
C.1molX的单质跟足量水反应时,发生转移的电子为2mol
D.Y的氢化物稳定性大于Z的氢化物稳定性
参考答案:D
本题解析:由元素在周期表中的位置可知X为He元素,Y为F元素,Z为S元素,则
A.Z为S元素,为非金属元素,故A错误;
B.Y为F元素,无正价,不存在最高价氧化物的水化物,故B错误;
C.X为He元素,性质稳定,不与水反应,故C错误;
D.非金属性:F>S,则稳定性:HF>H2S,故D正确.
故选D。
点评:本题考查元素的推断与周期律知识,题目难度不大,本题注意把握元素周期律的递变规律以及常见元素化合物的性质。
本题难度:简单
4、选择题 下列说法中,正确的是
A.离子化合物中,阴、阳离子间存在静电吸引力
B.HF、HCl、HBr和HI的热稳定性和还原性从左到右依次减弱
C.第三周期非金属元素对应的含氧酸从左到右依次增强
D.短周期元素形成离子后,最外层电子数都达到8电子稳定结构
参考答案:A
本题解析:离子化合物中,阴阳离子间存在着静电作用,其包括静电吸引和排斥,A对;四者的热稳定性从左到右逐渐减弱,但还原性是逐渐增强,B错;第三周期非金属元素的最高价含氧酸的酸性从左到右依次增强,C错;短周期元素原子转变成离子后,不一定是8电子稳定结构,比如氢离子根本没有电子,D错。
本题难度:一般
5、填空题 (10分)(1)在 H,
H,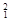 H,
H,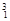 H,
H,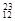 Mg,
Mg,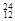 Mg,
Mg,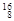 O,
O, O,
O,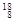 O中共有______种元素,______种原子,中子数最多的是?。D218O的相对分子质量是______。
O中共有______种元素,______种原子,中子数最多的是?。D218O的相对分子质量是______。
(2)人类的生活和生产活动,都离不开能源。在石油、电能、风能、煤碳、天然气、秸杆、水力、水煤气这些能源中,属于“二次能源”的(两种)是____,_??(共1分)属于“不再生能源”的(三种)是___?,?,?_(共1分)。
(3)化学反应的限度是当_?_____和?__相等,反应物和生成物的 _?____保持不变时,所达到的一种看似? 的“平衡状态”。
参考答案:(1) 3, 8,Mg,22
(2)电能、水煤气,石油、煤碳、天然气
(3)正反应速率,逆反应速率,浓度,静止
本题解析:(1)含有相同质子数原子属于同种元素,质子数或中子数不同即为不同的原子;
(2)化石能源不可再生
本题难度:简单