1��ѡ���� ����ʵ�鷽���У���������
A.������ʯ�ҳ�ȥ����������ˮ
B.��5?mL����1mLŨ��ˮ��Ӧ��Fe�������������屽
C.������Ũ���ᡢŨ����Ļ��������μ��뱽����50-60���ˮԡ�м�������ȡ������
D.��2.5g?���ӡ�2.5mL40%�ļ�ȩ��Һ��ϣ���ˮԡ�����Ʒ�ȩ��֬
�ο��𰸣�C
���������������A����ʯ�������ᷴӦ��
B������Һ���Ʊ��屽��
C�������ܶȱ�ˮС���Ʊ���������Ҫˮԡ���ȣ�
D�����ӹ�����Ӧ�����������£�
���A����ʯ�������ᷴӦ����������ʯ�ҳ�ȥ����������ˮ����A����
B������Һ���Ʊ��屽������������Ũ��ˮ����B����
C�������ܶȱ�ˮС����������Ũ���ᡢŨ����Ļ��������μ��뱽��Ȼ����50-60���ˮԡ�м����Ʊ�����������C��ȷ��
D�����ӹ�����Ӧ�����������£���2.5g?���ӡ�2.5mL40%�ļ�ȩ��Һ��ϣ��ټ���2mLŨ���ᣬȻ���ˮԡ�����Ʒ�ȩ��֬����D����
��ѡC��
���������⿼�黯ѧʵ�鷽�������ۣ��漰���ӡ����ʵ��Ʊ���ע�ⳣ��ˮԡ���ȵ�ʵ�飬ʵ��ϸ���ǿ�����ص㣬ѡ��DΪ�����ѵ㣬��Ŀ�ѶȽϴ�
�����Ѷȣ�����
2������� �Ӵ�����������Ŀǰ��ҵ�������������Ҫ��������ش��������⣺
��1����ҵ���ô˷�����������ʱ����Ҫ����Ҫԭ���п�����______��98.3%�����ᣮ
��2�������������в�����β��������о��������������ȿ��Խ�SO2����������SO3���ֿ�______�������г���Na2SO3��Һ����SO2β�����������£���1����������������Һ����SO2�������������ƣ���2������������Һ��ʹ֮���������������ƣ�ͬʱ�õ�______����Ʒ��
�ο��𰸣���1���Ӵ��������������ú������������ڷ���¯�к�������Ӧ���ɶ������������������Ϊ��������98.3% ���������յõ����ᣬ��ҵ���ô˷�����������ʱ����Ҫ����Ҫԭ���п�������������FeS2��S�ȣ���98.3% �����
�ʴ�Ϊ����������FeS2��S�ȣ���
��2��������������Ⱦ�Ե����壬�����ŷŵ������У���Ҫ���մ����������г���Na2SO3��Һ����SO2β�����������£���1����������������Һ����SO2�������������ƣ���2������������Һ��ʹ֮���������������ƣ�ͬʱ�õ�����Ũ��SO2��ˮ������
�ʴ�Ϊ����ֹSO2��Ⱦ����������Ũ��SO2��ˮ������
���������
�����Ѷȣ�һ��
3������� ij��Ϊ�ۺ�������������ʯ�ࣨCaSO4?2H2O����������¹��������Ʊ��������ʯ�ң�
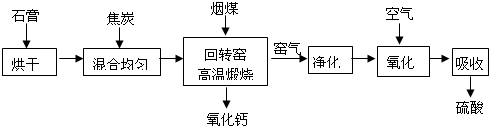
�ش��������⣺
��1��Ҥ���г�����CO2�⣬�����е���Ҫ������______��
��2��Ҥ���������������������չ����з�����Ӧ�Ļ�ѧ����ʽΪ______��
��3����תҤ�ڽ�̿������Ʒ�Ӧ�Ļ�ѧ����ʽΪ______��
��4���������Ʒ��������õ��ij���������һ�ַdz���Ч����ϴ����һ�������£����������Գ�ȥ�辧Ƭ�����е����������������������ȥ�辧Ƭ��ͭ�����Ļ�ѧ����ʽΪ______��
�ο��𰸣���1����̿��ʯ�����ܷ����Ļ�ѧ��Ӧ��������ʯ�ҡ�������̼�Ͷ�����������Ҥ���к���CO2��SO2���ʴ�Ϊ����������
��2�����������ܱ���������Ϊ������������������ˮ��Ӧ�õ����ᣬԭ������ʽΪ��2SO2+O2?2SO3��SO3+H2O=H2SO4���ʴ�Ϊ��2SO2+O2?2SO3��SO3+H2O=H2SO4��
��3����̿������Ʒ�Ӧ��������ʯ�ҡ�������̼�Ͷ���������ʽΪ��C+2CaSO4�T2CaO+CO2��+2SO2����
��4������ͭ������ϡ���ᣬ�����ܺ�Ũ���ᷴӦ��������Ũ�����ȥ�辧Ƭ��ͭ��������ӦΪ��Cu+2H2SO4�TCuSO4+SO2��+2H2O���ʴ�Ϊ��Cu+2H2SO4�TCuSO4+SO2��+2H2O��
���������
�����Ѷȣ�һ��
4��ѡ���� ��������ʵ�Ľ�����ȷ����
A.�������м���Ũ�������ַ�������˵��Ũ���������ˮ��
B.Ũ�����Ũ�����Ͽ����Ȼ��⣬˵��Ũ������һ���ѻӷ�����
C.�����£�Ũ����������������棬˵������Ũ�����Ӧ
D.��ӦCuSO4+H2S��CuS��+H2SO4�ܽ��У�˵����ͭ�Ȳ�����ˮ��Ҳ������ϡ����
�ο��𰸣�AD
���������������A��Ũ���������ˮ�ԣ���ʹ������ˮ����ڣ�
B������Ũ����ϡ��ʱ���ȣ��ӿ����Ȼ���Ļӷ���
C�������£�Ũ�������������ۻ���
D����Ӧ������֪�����������ᷴӦ������������ǿ�ᣮ
���A��Ũ���������ˮ�ԣ���ʹ������ˮ����̿�ڣ���A��ȷ��
B��Ũ�����Ũ�����Ͽ����Ȼ��⣬˵��Ũ������һ���ѻӷ����ᣬ��B����
C�������£�Ũ�������������ۻ����ڱ�������һ�����ܵ�������Ĥ�����Գ�����Ũ����������۳����ˣ���C��ȷ��
D�����������Ʊ�ǿ���������ԭ��������CuS�Ȳ�����ˮ��Ҳ������ϡ���ᣬ��D��ȷ��
��ѡAD��
���������⿼��Ũ��������ʣ���Ŀ�ѶȲ���ע��Ũ�������ˮ�ԡ���ˮ���Լ�ǿ�����Ե����ʣ�
�����Ѷȣ�һ��
5��ѡ���� ����ʵ���������ɻ�ʵ����ۺ�������
A.֤��һƿ����ɫ���������������Ƕ���������������ʪ��ĵ⻯��-������ֽ���飬�۲���ֽ��ɫ�ı仯
B.����ˮ��pH�������ò�����պȡ��ˮ���ڸ����pH��ֽ�ϣ������ɫ��ͱ���ɫ������
C.��������Ũ�����н��ݺ���������ˮ��ϴ��Ȼ�����CuSO4��Һ�в���Ӧ��˵�����������γ���һ�������ȶ�������Ĥ
D.��ij��Һ�м���ϡ���ᣬ�ܲ���ʹ����ʯ��ˮ����ǵ����壬˵������Һ��һ������CO32-
�ο��𰸣�C
���������������A����Ͷ������������������ԣ�
B����ˮ��ʹpH��ֽ��ɫ��
C������Ũ�����з����ۻ���
D���ܲ���������̼�IJ�һ��Ϊ̼���Σ�
���A����Ͷ������������������ԣ����������⻯�ض����ɵ��ʵ⣬��ķ����ǽ�����ͨ��ˮ�У���Һ��ɫ��Ϊ�����������壬��A����
B����ˮ����ǿ�����Ժ�Ư���ԣ��ɽ�pH��ֽƯ�ף�Ӧ��pH�Ʋⶨ����B����
C������Ũ�����з����ۻ����ڱ�������һ�����ܵ�������Ĥ���谭��Ӧ�ļ������У���C��ȷ��
D���ܲ���ʹ����ʯ��ˮ����ǵ��������Ϊ������̼������������壬��Һ�п��ܴ���CO32-��SO32-��HCO3-�ȣ���D����
��ѡC��
���������⿼�黯ѧʵ�鷽�������ۣ���Ŀ�Ѷ��еȣ�������ע��������ʵ�����ѡ��ʵ�鷽�����״���ΪB��ע����ˮ�ijɷּ����ʣ�
�����Ѷȣ�����