| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《盐类水解的原理》试题预测(2019年最新版)(六)
参考答案:B 本题解析: 本题难度:困难 2、选择题 下列物质中,水解的最终产物不能发生银镜反应的是( ? ) 参考答案:B 本题解析: 本题难度:简单 3、选择题 下列说法正确的是 |
参考答案:B
本题解析:
试题解析:一般弱酸的酸式强碱盐水溶液呈碱性,但也有显酸性的,如NaHSO3、NaH2PO4;另外强酸酸式盐水溶液显酸性,如NaHSO4,故A项错;溶液酸碱性取决于溶液中氢离子和氢氧根浓度的相对大小,氢离子浓度等于氢氧根浓度时,溶液呈中性,故B正确;NaHSO3属强碱弱酸盐,水解显酸性pH<7,Na2SO4属强酸强碱盐不水解,溶液显中性pH=7,故C错误;若反应生成的盐能水解,则中和后溶液不一定显中性,故D错误。
考点:溶液的酸碱性
本题难度:一般
4、填空题 某探究小组将一批电子废弃物简单处理后,得到含Cu、Al、Fe及少量Au、Pt等金属的混合物,并设计如下制备硫酸铜晶体和无水氯化铁的方案: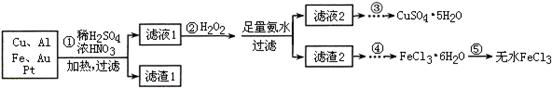
已知:Cu2+ + 4NH3・H2O=[Cu(NH3)4]2+ + 4H2O
请回答下列问题:
(1)步骤①Cu与酸反应的离子方程式为 。
(2)步骤②加H2O2的作用是 ,滤渣2为(填化学式) 。
(3)步骤⑤不能直接加热脱水的理由是 。
(4)若滤液1中Cu2+的浓度为0.02mol・L-1,则氢氧化铜开始沉淀时的pH =
(已知:Ksp[Cu(OH)2]=2.0×10-20)。
(5)已知:2Cu2++4I-= 2CuI↓+I2 I2+2S2O32-= 2I-+S4O62-
某同学为了测定CuSO4・5H2O产品的质量分数可按如下方法:取3.00g产品,用水溶解后,加入足量的KI溶液,充分反应后过滤、洗涤,将滤液稀释至250mL,取50mL加入淀粉溶液作指示剂,用0.080 mol・L-1 Na2S2O3标准溶液滴定,达到滴定终点的依据是 。
四次平行实验耗去Na2S2O3标准溶液数据如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液(mL) | 25.00 | 25.02 | 26.20 | 24.98 |
参考答案:(1)Cu + 4H+ + 2NO3? = Cu2+ +2NO2↑+ 2H2O 3Cu+8H++2NO3? 3Cu2++2NO↑+4H2O (任写一个给2分)
3Cu2++2NO↑+4H2O (任写一个给2分)
(2)将Fe2+氧化成Fe3+ (1分) Fe(OH)3、Al(OH)3 (各1分共2分)
(3)FeCl3易水解:FeCl3+3H2O  Fe(OH)3+3HCl,加热能促进FeCl3的水解,蒸干得不到FeCl3。(2分)
Fe(OH)3+3HCl,加热能促进FeCl3的水解,蒸干得不到FeCl3。(2分)
(4) 5 (2分)
(5)溶液由蓝色褪为无色且半分钟内不恢复原色 (2分) 83.3% (2分)
本题解析:(1)浓硝酸与稀硫酸混合后,可能为浓硝酸也可能为稀硝酸,所以离子方程式为:Cu + 4H+ + 2NO3? = Cu2+ +2NO2↑+ 2H2O或3Cu+8H++2NO3? 3Cu2++2NO↑+4H2O
3Cu2++2NO↑+4H2O
(2)H2O2具有强氧化性,所以H2O2的作用是将Fe2+氧化成Fe3+;加入足量氨水,Fe3+、Al3+转化为Fe(OH)3沉淀和Al(OH)3沉淀,所以滤渣2为Fe(OH)3、Al(OH)3。
(3)FeCl3为强酸弱碱盐,容易发生水解反应:FeCl3+3H2O  Fe(OH)3+3HCl,加热能促进FeCl3的水解,蒸干得不到FeCl3。
Fe(OH)3+3HCl,加热能促进FeCl3的水解,蒸干得不到FeCl3。
(4)c2(OH?)?c(Cu2+)= Ksp[Cu(OH)2],代入数据可求出c(OH?)=1.0×10-9mol?L?1,pH=-lgc(H+)=-lg【Kw÷c(OH?)】=5。
(5)Cu2+把I?氧化为I2,加入淀粉溶液变蓝,用Na2S2O3标准溶液滴定,达到滴定终点时,Na2S2O3与I2恰好完全反应,所以达到滴定终点的依据是:溶液由蓝色褪为无色且半分钟内不恢复原色;实验3所测数据明显大于其他3组数据,说明实验3出现了实验错误,应舍去,根据其他3组数据求出平均值,根据2Cu2++4I-= 2CuI↓+I2和I2+2S2O32-= 2I-+S4O62-可得对应关系:S2O32- ~ Cu2+,所以n(CuSO4?5H2O)=n(Cu2+)=n(S2O32- )=0.080 mol・L-1 ×(25.00+25.02+24.98)/3L=0.002mol,所以此产品中CuSO4・5H2O的质量分数为:0.002mol×250g/mol×5÷3.00g×100%=83.3%
考点:本题考查化学流程的分析、化学方程式的书写、盐类水解的应用、pH的计算、氧化还原反应滴定及计算。
本题难度:困难
5、选择题 在配置Fe2(SO4)3溶液时,为了防止水解,常常往溶液中加入少量的:( )
A.NaOH
B.H2SO4
C.KCl
D.CH3COOH
参考答案:B
本题解析:Fe2(SO4)3溶液中,三价铁易水解为氢氧化铁,实质是:Fe3++3OH-?Fe(OH)3+3H+,在配置Fe2(SO4)3溶液时,为了防止水解,常常往溶液中加入少量的硫酸,这样也不会再硫酸铁中引进新的杂质离子,(不能加除硫酸以外的酸)。
故选B。
考点:盐类水解的应用
点评:本题是一道水解原理的应用:溶液的配制知识题目,可以根据所学知识进行回答,难度不大。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点归纳《离子共存》.. | |