1、选择题 下列化学实验事实解释正确的是
[? ]
A.过量的铜屑与稀硝酸作用,反应停止后,再加入1mol/L稀硫酸,铜屑又逐渐溶解,是因为铜可直接与1mol/L稀硫酸反应
B.铁钉放在浓硝酸中浸泡后,再用蒸馏水冲洗,然后放入CuSO4溶液中不反应,说明铁钉表面形成了一层致密稳定的氧化膜
C.把SO2通入酸性高锰酸钾,紫红色褪色,可验证SO2的漂白性
D.常温下,将铜放入浓硫酸中无明显变化,说明铜在冷的浓硫酸中钝化
参考答案:B
本题解析:
本题难度:一般
2、选择题 向盛有FeCl3、CuCl2混合溶液的小烧杯中,加入一定量的铁粉,充分反应后,烧杯中有固体剩余,下列有关说法正确的是( )
A.剩余固体一定是铁
B.剩余固体一定是铜
C.反应后溶液中一定有Fe2+
D.反应后溶液中滴入KSCN溶液可能变成红色
参考答案:C
本题解析:
本题难度:简单
3、选择题 某课外实验小组设计的下列实验不合理的是( )
A.
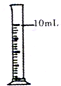
准确量取7.60ml盐酸
B.

实验室制备少量氨气
C.
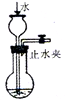
检查装置气密性
D.
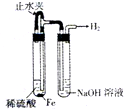
制备并观察氢氧化亚铁
参考答案:A
本题解析:
本题难度:简单
4、实验题 (共6分,每空2分)铜是日常生活中常见的金属。已知铜的原子序数为29。回答问题:
 (1)铜是不活泼的金属,不会和稀硫酸反应,但在盛有铜和稀硫酸的试管中加入双氧水以后,能够看到铜溶解。请写出该反应的离子方程式?。
(1)铜是不活泼的金属,不会和稀硫酸反应,但在盛有铜和稀硫酸的试管中加入双氧水以后,能够看到铜溶解。请写出该反应的离子方程式?。
 (2)如果不加氧化剂实现铜在稀硫酸溶液中的溶解,请设计一个实验装置完成此过程。在方框中画出该装置。
(2)如果不加氧化剂实现铜在稀硫酸溶液中的溶解,请设计一个实验装置完成此过程。在方框中画出该装置。
?
 (3)写出你所设计装置中的化学反应的方程式?。
(3)写出你所设计装置中的化学反应的方程式?。
参考答案:
 (1)Cu+H2O2+2H+ =Cu2+ +2H2O
(1)Cu+H2O2+2H+ =Cu2+ +2H2O
 (2)
(2)
通电
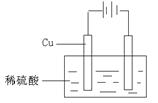
 (3)Cu+H2SO4 == CuSO4 +H2↑
(3)Cu+H2SO4 == CuSO4 +H2↑
本题解析:略
本题难度:简单
5、填空题 (14分)利用废铁丝、硫酸铜废液(含硫酸亚铁)和被有机物污染的废铜粉制备硫酸铜晶体。生产过程如下:

试回答下列问题:
(1)铁丝在投入硫酸铜废液前需用稀H2SO4进行处理,可能发生反应的离子方程式有?。
(2)为了使灼烧后的氧化铜混合物充分酸溶,在加入稀H2SO4的同时,还通入O2。通入O2的目的是(用化学反应方程式表示)?。
在实验室中,常将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示)。
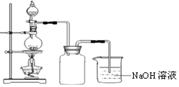
(3)写出烧瓶中发生反应的离子方程式为?
(4)广口瓶的作用是?
(5)为符合绿色化学的要求,某研究性学习小组进行如下
设计:将3.2 g铜丝放到45 mL 1.5 mol・L-1的稀硫酸中,控温在50 ℃。加入18 mL 10%的H2O2,反应0.5h后,升温到60 ℃,持续反应1 h后,过滤、蒸发浓缩、减压抽滤等,用少量95%的酒精淋洗后晾干,得CuSO4・5H2O 10.5 g。请回答:
①加热时温度不宜过高的原因是?;
②本实验CuSO4・5H2O的产率为?。
参考答案:⑴? Fe2O3+6H+=2Fe3++3H2O,2Fe3++Fe=3Fe2+,Fe+2H+=Fe2++H2↑;
⑵ 2Cu+O2+2H2SO4=2CuSO4+2H2O 或2Cu+O2=2CuO,CuO+H2SO4=CuSO4+H2O ;
⑶ 3Cu+8H++3NO3-?=3Cu2++2NO↑+4H2O ;
⑷ 安全瓶 ;⑸? ①防止双氧水分解 ;②84% 。
本题解析:(1)铁丝表面有铁锈。投入稀H2SO4中发生反应的两种方程式为:Fe2O3+6H+=2Fe3++3H2O;2Fe3++Fe=3Fe2+;Fe+2H+=Fe2++H2↑;(2)为了使灼烧后的氧化铜混合物充分酸溶,在加入稀H2SO4的同时,还通入O2。通入O2的目的是使Cu变为氧化铜,与酸反应得到CuSO4.反应的方程式为:2Cu+O2+2H2SO4=2CuSO4+2H2O 或2Cu+O2=2CuO,CuO+H2SO4=CuSO4+H2O ;(3)在烧瓶中Cu与稀硝酸发生反应的离子方程式为:3Cu+8H++3NO3-?=3Cu2++2NO↑+4H2O ;(4)广口瓶的作用是安全瓶,防止倒吸现象的发生;(5)①加热时温度不宜过高是由于在反应的过程中使用了H2O2,而H2O2受热容易分解,使用温度不宜过高。②n(Cu)=" 3.2" g÷64g/mol=0.05mol,n(H2SO4)=" 0.045" L×1.5 mol/L=" 0.0675" mol硫酸过量,所以产生的CuSO4按照Cu来计算,理论产量:0.05mol×250g/mol=12.5g。因此CuSO4・5H2O的产率为(10.5 g÷12.5g)×100%=84%。
本题难度:一般