1、填空题 工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:
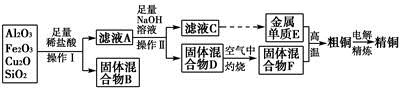
已知:Cu2O+2H+=Cu+Cu2++H2O
(1)实验操作Ⅰ的名称为________;在空气中灼烧固体混合物D时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有________(填仪器名称)。
(2)滤液A中铁元素的存在形式为________(填离子符号),生成该离子的离子方程式为____________________________________________,检验滤液A中存在该离子的试剂为________(填试剂名称)。
(3)金属单质E与固体混合物F发生的某一反应可用于焊接钢轨,该反应的化学方程式为__________________________________________________。
(4)常温下,等pH的NaAlO2和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍。则两种溶液的pH=________。
(5)从浓硫酸、浓硝酸、蒸馏水中选用合适的试剂,测定粗铜样品中金属铜的质量分数,涉及的主要步骤:称取一定质量的样品→________________→过滤、洗涤、干燥→称量剩余固体铜的质量。(填缺少的操作步骤,不必描述操作过程的细节)
参考答案:(1)过滤 坩埚
(2)Fe2+ 2Fe3++Cu=2Fe2++Cu2+ 硫氰化钾溶液和新制氯水(合理的氧化剂均可)
(3)2Al+Fe2O3 Al2O3+2Fe (4)11
Al2O3+2Fe (4)11
(5)将浓硫酸用蒸馏水稀释,将称得的样品与足量稀硫酸充分反应
本题解析:由流程图可以看出,加入足量稀盐酸时,得到的固体混合物B为二氧化硅和单质铜,则滤液A中一定不含Fe3+,原因是2Fe3++Cu=2Fe2++Cu2+,验证Fe2+可先加入KSCN溶液,没有明显现象,再加入氯水(或其他氧化剂)出现血红色。滤液A中含有Fe2+、Al3+、Cu2+,加入足量NaOH溶液后得到的固体混合物D为Fe(OH)3和Cu(OH)2,在空气中灼烧后得到的固体混合物F为Fe2O3和 CuO,滤液C中含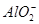 ,则金属单质E为Al,利用铝热反应可焊接钢轨。(4)NaAlO2溶液中水的电离受到促进,而NaOH溶液中水的电离受到抑制。设两种溶液的pH=a,NaAlO2溶液中水电离出的c(OH-)为10a-14mol・L-1,NaOH溶液中水电离出的c(OH-)为10-amol・L-1,10a-14=108×10-a,得a=11。(5)用稀H2SO4溶解粗Cu中的活泼金属。
,则金属单质E为Al,利用铝热反应可焊接钢轨。(4)NaAlO2溶液中水的电离受到促进,而NaOH溶液中水的电离受到抑制。设两种溶液的pH=a,NaAlO2溶液中水电离出的c(OH-)为10a-14mol・L-1,NaOH溶液中水电离出的c(OH-)为10-amol・L-1,10a-14=108×10-a,得a=11。(5)用稀H2SO4溶解粗Cu中的活泼金属。
本题难度:一般
2、选择题 下列有关金属的说法中,不正确的是
A.钠是一种强还原剂,可以把钛、锆、铌等从其熔融盐中置换出来
B.镁铝合金常用作宇宙飞船、火箭、导弹、飞机中某些部件的金属材料
C.铜能与氯化铁溶液反应,该反应可应用于印刷电路板的制作
D.铁能与硫酸发生反应,不能用铁制容器贮存浓硫酸
参考答案:D
本题解析:在常温下,铁在浓硫酸中发生钝化,所以能用铁制容器贮存浓硫酸,选项D不正确,其余选项都是正确的,答案选D。
点评:该题是常识性知识的考查,难度不大。该题的关键是记住常见金属的性质、用途,特别是化学性质,然后结合题意灵活运用即可,有利于培养学生的学习兴趣,增强学生的学习自信心。
本题难度:一般
3、选择题 下列金属的冶炼方法不正确的是: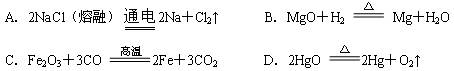
参考答案:B
本题解析:略
本题难度:简单
4、选择题 将过氧化钠投入到氯化亚铁溶液中,可观察到的现象是(?)
A.最终生成白色沉淀
B.最终生成红褐色沉淀
C.最终出现灰绿色沉淀
D.无变化
参考答案:B
本题解析:过氧化钠具有强氧化性可以将亚铁氧化为三价铁,投入氯化亚铁溶液中时与水先反应生成氢氧化钠,再生成氢氧化铁沉淀,红褐色的沉淀,所以答案选B。
本题难度:简单
5、选择题 常温下,不能用铁制容器存放的物质是
A.浓硫酸
B.浓硝酸
C.CuSO4溶液
D.稀氨水
参考答案:C
本题解析:浓硫酸、浓硝酸都可以使铁制容器发生钝化能用铁制容器存放,A、B不选;
CuSO4+Fe=" Fe" SO4+ Cu?,CuSO4溶液不能用铁制容器存放,稀氨水不与铁反应可用铁制容器存放。答案选C.
本题难度:简单