1、选择题 事实上,许多非金属氧化物在一定条件下能与Na2O2反应,且反应极有规律.如:
Na2O2+SO2===Na2SO4、2Na2O2+2SO3===2Na2SO4+O2↑,据此,你认为下列方程式中不正确的是
[? ]
A.2Na2O2+2Mn2O7===4NaMnO4+O2↑
B.2Na2O2+P2O3===Na4P2O7
C.2Na2O2+2N2O3===4NaNO2+O2↑
D.2Na2O2+2N2O5===4NaNO3+O2↑
参考答案:C
本题解析:
本题难度:简单
2、计算题 (6分)将一定量的碳酸钠和碳酸氢钠的混合物27.4 g,跟含溶质0.4mol 的盐酸恰好反应,生成二氧化碳气体。
(已知碳酸氢钠和盐酸反应的方程式如下:NaHCO3+HCl→NaCl+CO2↑+H2O )
(1)写出碳酸钠与盐酸反应的化学方程式
(2)求原混合物中碳酸钠和碳酸氢钠的质量各多少克?
(3)求生成的二氧化碳气体在标准状况下的体积。
参考答案:(6分)
(1)Na2CO3+2HCl→2NaCl+CO2↑+H2O
(2)10.6克 16.8克(3)6.72升
本题解析:略
本题难度:一般
3、计算题 将2.5g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol・L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
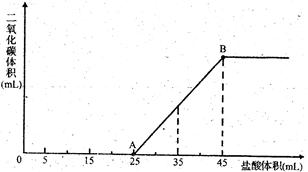
(1)写出OA段所发生反应的离子方程式:?;
(2)当加入35mL盐酸时,产生二氧化碳的体积为?mL(标准状况);
(3)原混合物中Na2CO3的质量分数为?。
参考答案:(1)OH-+H+=H2O(1分)H++CO2-3=HCO-3(1分)
(2)224(2分)
(3)42.4%(2分)
本题解析:略
本题难度:简单
4、选择题 10 g碳酸钙样品(内含一种杂质)与足量盐酸反应得到4.3 g CO2,则碳酸钙中可能含有(? )
A.MgCO3
B.Na2CO3
C.NaHCO3
D.K2CO3
参考答案:BD
本题解析:10 g纯CaCO3与足量盐酸的反应可产生4.4 g CO2,显然10 g杂质产生CO2的质量必小于4.3 g。
本题难度:简单
5、选择题 纯碱和小苏打的主要成分分别是碳酸钠和碳酸氢钠。要在家庭中将它们区分开来,下面方法可行的是
A.分别将两种样品放在钞锅中加热,观察锅底是否有残留物
B.分别用干净铁丝蘸取样品在煤气炉的火焰上灼烧,观察火焰颜色
C.在盛有两种样品的水杯中分别加入食醋,观察反应的剧烈程度
D.将两种样品分别溶解,并滴加澄清石灰水,观察是否有白色沉淀
参考答案:C
本题解析:略
本题难度:简单