1��ѡ���� ��ˮ��Һ���ܴ��������һ����
[? ]
A.?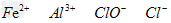 ?
?
B.?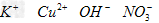 ?
?
C.? ?
?
D.?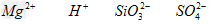 ?
?
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2������� ����п���Ʊ�ӫ��۵�ԭ��֮һ����ҵ����п����Ҫ�ɷ���ZnO��������Fe2O3��CuO��SiO2�����ʣ��Ʊ�ZnSO4?7H2O���������¡�
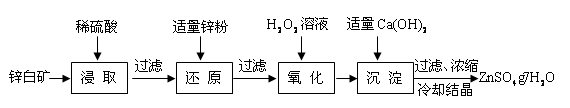
��֪�������£���Һ�е�Fe3+��Zn2+��Fe2+������������ʽ��ȫ������pH�ֱ�Ϊ��3.7��6.5��9.7��
��1����ȡ��������߽���Ч�ʿɲ��õĴ�ʩ���������δ�һ������
ZnO�����ᷴӦ�Ļ�ѧ����ʽΪ������
��2����������п�۵�����Ϊ����ʹ��Һ�е�Fe3+ת��ΪFe2+����������
��3������������H2O2������Ӧ�����ӷ���ʽΪ������
��4����������Ca(OH)2������ҺpH���ٽ�Fe3+ˮ�⣬Fe3+ˮ�ⷴӦ��ƽ�ⳣ������ʽ
K��������Ca(OH)2���ܹ�����ԭ����������
�ο��𰸣���12�֣�
��1������ʯ�������߽�ȡ�¶Ȼ��ʵ��������Ũ�ȵȣ�2�֣�?
ZnO+H2SO4=ZnSO4+H2O��2�֣�
��2����ȥCu2+��2�֣�
��3��H2O2+2Fe2++2H+=2Fe3++2H2O��2�֣�
��4��c3(H+)/c(Fe3+) ��2�֣�?��ֹ����Zn(OH)2��2�֣�
�����������1��������������ͬ�����������Ҫ�ɷݷ�Ӧ���ӻ�ѧ��Ӧ���ʺͻ�ѧƽ���Ӱ��������������ͨ�������¶��������п���ܽ�ȣ���ͨ������ʹ��Ӧ���ֽӴ���Ӧ����ͨ�����˺�������ν�ȡ�����ת���ʣ��ʴ�Ϊ���ʵ���߷�Ӧ�¶ȡ����ӽ���ʱ�䣨�����������𰸣���ZnO�����ᷴӦ�Ļ�ѧ����ʽΪZnO+H2SO4=ZnSO4+H2O���ʴ�Ϊ�� ZnO+H2SO4=ZnSO4+H2O���Ƽ���п�ۣ��������·�Ӧ��Zn��2H��=Zn2����H2����Zn��2Fe3��=2Fe2����Zn2�� ,Fe��Cu2�� =Cu��Zn2�� ,Zn������Fe2����Zn=Fe��Zn2�� ��������Ŀ�м���������п�ۣ��ڳ�ȥCu2�� ���𰸣���ȥCu2+����H2O2��Fe2�� ������Fe3�� ������pH�ϵ͵������£�����ˮ���ȥFe3�� ���𰸣�H2O2+2Fe2++2H+=2Fe3++2H2O���ȸ���ˮ�ⷽ��ʽFe3����3H2O Fe(OH)3��3H�� ,д��ƽ�ⳣ��K= c3(H+)/c(Fe3+) ��Ca(OH)2���ܹ�����ԭ���ǣ�Fe3�� ��pHΪ1.1�D3.2ʱ������pH��5.9�D8.9ʱZn2�� �������𰸣�c3(H+)/c(Fe3+)����ֹ����Zn(OH)2��
Fe(OH)3��3H�� ,д��ƽ�ⳣ��K= c3(H+)/c(Fe3+) ��Ca(OH)2���ܹ�����ԭ���ǣ�Fe3�� ��pHΪ1.1�D3.2ʱ������pH��5.9�D8.9ʱZn2�� �������𰸣�c3(H+)/c(Fe3+)����ֹ����Zn(OH)2��
�����Ѷȣ�����
3������� �����е������֣�K+��NH+4��Cl-��Mg2+��Ba2+��CO23��SO2-4����ȡ������Һ��������ʵ�飺
��1����һ�ݼ���AgNO3��Һ�г������ɡ�
��2���ڶ��ݼ�������NaOH��Һ�����Ⱥ��ռ�������0.04mol��
��3�������ݼ�������BaCl2��Һ�ø������6.27g������������ϴ�ӣ������������Ϊ2.33g����������ʵ�飬�����жϣ�
��Һ��һ�����ڵ�������?
����Һ��һ�������ڵ�������?
����Һ�п��ܴ��ڵ�������?
�ο��𰸣�CO2-3��SO2-4��NH+4��K+��Mg2+��Ba2+��Cl-��
�����������
�����Ѷȣ�һ��
4��ѡ���� ����Һ�м�������Na2O2�����ܴ���������������ǣ�������
A��NH4+��Ba2+��Cl-��NO3-
B��K+��AlO2-��Cl-��SO42-
C��Ca2+��Mg2+��NO3-��HCO3-
D��Na+��Cl-��CO32-��SO32-
�ο��𰸣�A��NH4+��OH-��Ӧ�����ܴ������棬��A����
B���ڼ��������£�����֮�䲻�����κη�Ӧ���ɴ������棬��B��ȷ��
C��Mg2+��OH-��Ӧ��Ca2+��HCO3-��OH-��Ӧ���ɳ��������ܴ������棬��C����
D��SO32-���л�ԭ�ԣ�����Na2O2����������ԭ��Ӧ����D����
��ѡB��
���������
�����Ѷȣ���
5��ѡ���� ���и������ӣ���ָ�������£�һ�����ܴ����������(? )
����������Ӧ����H2����Һ�У�Fe2+��Cl-��NH4+��NO3-
��pH��8.4����������Һ�У�Na+��K+��AlO2-��HCO3-
����ʹpH��ֽ������ɫ����Һ�У�Na+��K+��AlO2-��CO32-
����c(H+): c(OH-)��1:1012����Һ�У�Na+��I-��NO3-��SO42-
�ݳ�����ˮ�������c(H+)��c(OH-)��1:10-20����Һ�У�Na+��Cl-��S2-��SO32-
��ˮ�������c(H+)��1��10-12mol/L����Һ�У�Fe3+��NH4+��Cl-��NO3-
A���٢�
B���٢�
C���ڢ�
D���٢ڢݢ�
�ο��𰸣�B
���������������Һ���������ԣ�Ҳ�����Լ��ԣ����ܴ������档AlO2-��HCO3-������Ӧ�������������������ڲ��ܴ������档��ʹpH��ֽ������ɫ����Һ���Լ��ԣ����Դ������档c(H+): c(OH-)��1:1012����Һ��˵���Լ��ԣ����Դ������档ˮ�������c(H+)��c(OH-)��1:10-20����Һ��˵����Һ���������ԣ�Ҳ�����Լ��ԣ����Լ����ܴ������档ˮ�������c(H+)��1��10-12mol/L����Һ��˵��ˮ�ĵ��뱻���ƣ���Һ���������ԣ�Ҳ�����Լ��ԣ����������ܴ������档��ѡB��
�����Ѷȣ�һ��