1、选择题 无色透明溶液中,下列各组离子可以大量共存的是(?)
A.Ca2+、HCO3-、K+、Cl-
B.SO42-、Cl-、Ba2+、K+
C.Na+、H+、 SO32-、MnO4-
D.Na+、HCO3-、Ca2+、H+
参考答案::A
本题解析:B组SO42- 与Ba2+ 生成硫酸钡沉淀不共存;C组H+与 SO32-生成亚硫酸弱电解质不共存;D组HCO3-与H+生成二氧化碳和水不共存。
点评:离子间相互反应不能大量共存
1.相互结合生成沉淀。如:Ba2+和SO42-, Ag+和Cl-, Cu2+ 和OH-。
2.相互结合形成挥发性物质。如:H+和S2-、HS- 、CO32-、HCO32-、SO32-、HSO3-等。
3.离子间相互结合成弱电解质。如:H+和OH-、PO43-弱酸根等。
4.弱酸根与弱碱的阳离子会发生双水解反应。如:S2-和Al3+ , Fe3+ 和CO32-。
5.离子间发生氧化还原反应。如:Fe3+和S2-、I-, MnO4-和Fe2+、S2-、I-、SO32-等。
6.离子间相互结合形成络离子。如:Fe3+与SCN-形成 [Fe(SCN)]2+络离子
二.特殊条件要求某些离子不能大量共存
1.无色溶液中,则有色离子不能大量共存:如:Cu2+、Fe2+、Fe3+、MnO4-均是有色离子。
2.强酸性溶液,则非强酸根离子、OH-不能大量共存。如:PH=1的溶液中,OH-、S2-、HS-、CO32-、HCO3- 、SO32- 、HSO3-、ClO-、F-、PO43-、HPO42- 、S2O32- 等不能大量存在。
3.强碱性溶液中则H+、酸式根(如HCO3-、HSO3-、HS- )、非强碱的阳离子不能大量共存。如:PH=13的溶液中,H+、Cu2+、HCO3-等不能大量共存。
本题难度:一般
2、填空题 水的电离平衡曲线如图所示:
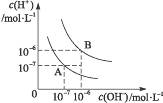
(1)若以A点表示25 ℃时水的电离平衡时的离子浓度,当温度升高到100 ℃时,水的电离平衡状态到B点,则此时水的离子积从____________________增加到_____________________。
(2)将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持100 ℃的恒温,致使混合液的pH=7,则Ba(OH)2与盐酸的体积之比为________________________________。
(3)已知AnBm的离子积=[C(Am+)]n・[C(Bn-)]m,式中的C(Am+)、C(Bn-)表示离子的物质的量浓度。若某温度下CA(OH)2溶解度为0.74 g,其饱和溶液密度设为1 g・mL-1,其离子积约为_____________________________________________。
参考答案:(1)1×10-14? 1×10-12? (2)2∶9? (3)0.004
本题解析:100 ℃时,pH=6是中性溶液,(2)中的混合溶液pH=7呈碱性,则c(OH-)=10-7 mol・L-1
=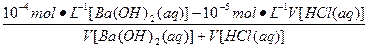 ,
,
整理即可得出二者体积比。(3)中Ca(OH)2的离子积=c(Ca2+)・〔c(OH-)〕2,c〔Ca(OH)2〕=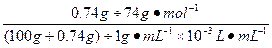 ≈0.1 mol・L-1,故c(Ca2+)="0.1" mol・L-1,c(OH-)="0.2" mol・L-1,代入上式即可解出Ca(OH)2的离子积。
≈0.1 mol・L-1,故c(Ca2+)="0.1" mol・L-1,c(OH-)="0.2" mol・L-1,代入上式即可解出Ca(OH)2的离子积。
本题难度:简单
3、选择题 室温下,下列各组离子在指定溶液中能大量共存的是
[? ]
A.饱和氯水中 Cl-、NO3-、Na+、SO32-
B.c(H+)=1.0×10-13mol/L溶液中 C6H5O-、K+、SO42-、Br-
C.Na2S溶液中 SO42-、K+、Cl-、Cu2+
D.pH=12的溶液中 NO3-、I-、Na+、Al3+
参考答案:B
本题解析:
本题难度:一般
4、选择题 下列可以大量共存且溶液是无色的离子组是( )
A.H+、Na+、NO3-、Cu2+
B.Ba2+、Mg2+、Cl-、SO42-
C.H+、K+、OH-、NO3-
D.NO3-、SO42-、K+、Mg2+
参考答案:D
本题解析:A. Cu2+离子在溶液中显蓝色A不符题意;
B.Ba2+和SO42-会反应生成BaSO4沉淀,B不符题意;
C.H+和OH-不能大量共存,C不符题意;?
D.NO3-、SO42-、K+、Mg2+可以大量共存且溶液是无色,D正确,故选D。
点评:本题考查离子间的反应及各种物质在水溶液中的颜色,题目难度不大。
本题难度:简单
5、选择题 下列各组离子在指定溶液中能大量共存的是( )
A.在无色溶液中: Na+、Mg2+、NO3ˉ、MnO4-
B.在含有HCO3-的溶液中:Al3+、K+、SO42-、Cl-
C.在pH=1的溶液中:K+、Na+、Iˉ、NO3ˉ
D.在强酸性的透明溶液中:Cu2+、K+、NO3ˉ、SO42-