1、选择题 用等质量的金属钠进行下列实验,其中生成氢气最多的是(?)
A.把钠放入足量稀盐酸中
B.将钠用铝箔包好并刺些小孔,再放入水中
C.把钠放入硫酸铜溶液中
D.把钠放入足量水中
参考答案:B
本题解析:略
本题难度:简单
2、填空题 有A、B、C、D四种钠的化合物,根据下列反应式判断A、B、C、D的化学式。
A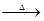 B+CO2+H2O ;D+CO2
B+CO2+H2O ;D+CO2 B+O2 ;D+H2O
B+O2 ;D+H2O C+O2↑;
C+O2↑;
B+Ca(OH)2 C+CaCO3↓。
C+CaCO3↓。
(1)写出A、B、C、D的化学式:A__________,B_________,C__________,D__________。
(2)1mol D 与足量CO2反应生成标准状况下的O2 的体积为_____。
参考答案:(1)NaHCO3 、Na2CO3、NaOH、Na2O2?(2)? 11.2L
本题解析:由于四种物质都含有钠元素,所以根据转化关系可知,A是碳酸氢钠,B是碳酸钠,C是氢氧化钠,D是过氧化钠。过氧化钠和CO2反应的方程式为2Na2O2+2CO2=2Na2CO3+O2,所以1mol过氧化钠生成0.5mol氧气,在标准状况下的体积是0.5mol×22.4L/mol=11.2L。
本题难度:一般
3、选择题 过氧化氢水溶液俗称双氧水,过氧化氢易分解为水和氧气,常作氧化剂、漂白剂和消毒剂,为贮存、运输、使用的方便,工业常将H2O2转化为过碳酸钠晶体(其化学式为2Na2CO3.3H2O2),它具有Na2CO3和H2O2的双重性质。下列物质不会使过碳酸钠晶体失效的是
A.MnO2
B.H2S
C.稀盐酸
D.NaHCO3
参考答案:D
本题解析:A项:MnO2做为催化剂,能加速H2O2分解而失效,故错;B项:H2O2能氧化H2S而失效,故错;C项:稀盐酸与Na2CO3反应而失效,故错。故选D。
点评:本题考查的是无机反应的知识,分析清楚发生化学反应的原理是解题的关键,题目难度不大。
本题难度:一般
4、实验题 在课堂上,老师演示了金属钠与CuSO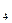 溶液的反应,同学们观察到该反应中生成了蓝色的Cu(OH)
溶液的反应,同学们观察到该反应中生成了蓝色的Cu(OH)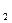 沉淀而没有发现铜单质生成。但某同学想:会不会因生成的铜较少被蓝色沉淀所覆盖,而没有被发现呢?于是他想课后到实验室继续研究,希望进一步用实验来验证自己的猜测是否正确。
沉淀而没有发现铜单质生成。但某同学想:会不会因生成的铜较少被蓝色沉淀所覆盖,而没有被发现呢?于是他想课后到实验室继续研究,希望进一步用实验来验证自己的猜测是否正确。
假如该同学是你,请你写一张实验准备单交给老师,要求老师提供必需的用品。
(1)实验探究目的:___________________________。
(2)探究所依据的化学原理:____________________________。
(3)实验必需仪器:小刀、玻璃片、滤纸、_________和__________;药品:金属钠、_____和___________。该同学在探究实验中意外地发现生成的蓝色沉淀中混有少量的黑色难溶物,而所使用的药品均没有问题,你认为该黑色难溶物是___________,生成该黑色难溶物的原因是_______________________________________________。
参考答案:(1)确定钠与CuSO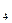 溶液反应是否有铜生成
溶液反应是否有铜生成
(2)氢氧化铜可溶于盐酸而铜不溶〔Cu(OH)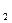 +2HCl
+2HCl CuCl
CuCl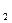 +2H
+2H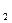 O〕
O〕
(3)镊子烧杯CuSO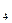 溶液盐酸(或稀硫酸)CuO 钠与水反应放出的热使生成的Cu(OH)
溶液盐酸(或稀硫酸)CuO 钠与水反应放出的热使生成的Cu(OH)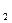 部分分解:Cu(OH)
部分分解:Cu(OH)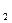
 CuO+H
CuO+H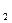 O
O
本题解析:欲探究钠与CuSO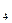 溶液反应是否置换出铜,应从Cu与Cu(OH)
溶液反应是否置换出铜,应从Cu与Cu(OH)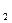 的不同性质入手,最简单的实验是将沉淀分离出来后用盐酸溶解,依此方案可确定所需的仪器和药品。
的不同性质入手,最简单的实验是将沉淀分离出来后用盐酸溶解,依此方案可确定所需的仪器和药品。
至于黑色难溶物,只可能是CuO,其解释便是Cu(OH)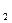 分解了。实际上,在实验中如果散热不快,很容易出现此现象。
分解了。实际上,在实验中如果散热不快,很容易出现此现象。
本题难度:简单
5、填空题 以下是对金属及其化合物的讨论,根据要求回答问题
(1)写出钠与水反应的离子方程式?。
(2)在AlCl3溶液中逐滴滴入过量的NaOH溶液,观察到的现象是?,
反应的离子方程式为?,?。
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为?。
参考答案:(1)2Na+2H2O=2Na++2OH-+H2↑?(2)先沉淀后溶解,Al3++3OH-=3Al(OH)3↓
Al(OH)3+OH-=AlO2-+2H2O?(3)1:1
本题解析:(1)书写离子方程式时,只能将强电解质(指溶于水中的强电解质)写出离子形式,其它(包括难溶强电解质)一律写成分子形式。则得出离子方程式为2Na+2H2O=2Na++2OH-+H2↑。(2)在AlCl3溶液中逐滴滴入NaOH溶液,先发生AlCl3+3NaOH=Al(OH)3↓+3NaCl,生成白色的Al(OH)3沉淀,随着NaOH溶液滴加过量,则生成的Al(OH)3与过量的NaOH反应生成NaAlO2,反应方程式为Al(OH)3+NaOH=NaAlO2+2H2O,沉淀又溶解。根据离子方程式书写规则得反应的离子方程式为Al3++3OH-=3Al(OH)3↓ Al(OH)3+OH-=AlO2-+2H2O (3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,而Al反应产生H2实质上是电子的转移,Al失电子,H+得电子变为H2,在相同状况下产生氢气的量相同,则由得失电子守恒知,消耗铝的物质的量也相同,因此,两个反应中消耗的铝的物质的量之比为1:1。
本题难度:一般