1、选择题 NaHCO3和Na2O2按1∶1的个数之比混合,在密闭容器中加热使之充分反应,然后趁热排出气体物质,容器内残留物的成分是
A.Na2O2和NaHCO3
B.NaHCO3和Na2CO3
C.NaOH和Na2CO3
D.只有Na2CO3
参考答案:C
本题解析:NaHCO3和Na2O2按1∶1的个数之比混合,在密闭容器中加热使之充分反应,NaHCO3分解生成CO2和H2O,根据化学方程式可知,CO2和H2O与Na2O2恰好反应,所以容器内残留物的成分为NaOH和Na2CO3,故C项正确。
本题难度:一般
2、填空题 碳酸钠俗称纯碱,其用途很广。实验室中,用碳酸氢铵和饱和食盐水可制得纯碱。各物质在不同温度下的溶解度见表。
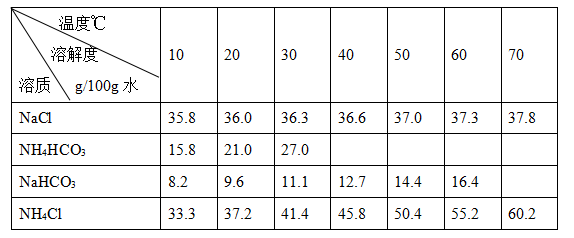
实验步骤
Ⅰ、化盐与精制:①粗盐(含Ca2+、Mg2+、SO42-)溶解;②加入足量NaOH和Na2CO3溶液,煮沸;③过滤;④加入盐酸调pH至7。
Ⅱ、转化:①将精制后的食盐溶液温度控制在30~35℃之间;在不断搅拌下,加入研细的碳酸氢铵;保温,搅拌半小时;②静置,a 、b ;③得到NaHCO3晶体。
Ⅲ、制纯碱:将得的NaHCO3放入蒸发皿中,在酒精灯上灼烧,冷却到室温,即得到纯碱。
完成下列填空:
(1)“化盐与精制”可除去的粗盐中的杂质离子是?。
(2)“转化”的离子方程式是?。
(3)“转化”过程中,温度控制在30~35℃之间的加热方式是?;为什么温度控制在30~35℃之间??。
(4)a、b处的操作分别是?、?。
(5)实验室制得的纯碱含少量NaCl还可能含少量NaHCO3,为测定纯碱的纯度,用电子天平准确称取样品G克,将其放入锥形瓶中用适量蒸馏水溶解,滴加2滴酚酞,用c mol/L的标准盐酸滴定至溶液由浅红色变成无色且半分钟不变,滴定过程中无气体产生,所用盐酸的体积为V1mL。此时发生的反应为:
CO32-+H+→HCO3-
①样品中碳酸钠质量百分含量的表达式是?。
②向锥形瓶溶液中继续滴加2滴甲基橙,用同浓度的盐酸继续滴定至终点,所用盐酸的体积为V2mL。滴定终点时溶液颜色的变化是?;根据实验数据,如何判断样品含NaHCO3?。
参考答案:(1)Ca2+、Mg2+
(2)Na++HCO3-→NaHCO3↓
(3)水浴加热;温度过高造成NH4HCO3分解,温度过低NH4HCO3的溶解度小
(4)过滤洗涤
(5)①Na2CO3%=(106cV1×10-3)/G
②黄色变为橙色且半分钟不变;V2>V1则含有NaHCO3
本题解析:(1)足量NaOH可以除去Mg2+;Na2CO3可以除去Ca2+;
(2)Na++HCO3-→NaHCO3↓
(3)根据水浴加热,温度易控制且受热均匀;温度过高造成NH4HCO3分解,温度过低,NH4HCO3的溶解度小;
(4)NH4HCO3与NaCl反应生成NaHCO3,便有晶体析出,然后过滤、洗涤可得到NaHCO3。
(5)①酚酞做指示剂,用浓度为cmol/LHCl溶液滴定至溶液由红色变成无色,说明CO32-+H+→HCO3-反应达到终点,所用盐酸的体积为V1mL,则碳酸钠的质量为106cV1×10-3g,其质量分数是(106cV1×10-3)/G。
②用甲基橙做指示剂,继续用HCl滴定至溶液由黄色变成橙色,则HCO3-+H+=CO2+H2O反应达到终点,所用HCl的体积为V2,如果V1=V2,只有Na2CO3;如果V2>V1,则含有NaHCO3。
本题难度:困难
3、选择题 ①钾的密度比水小;②钾的熔点较低;③钾与水反应时要放出热量;④钾与水反应后溶液呈碱性。某学生将一小块金属钾投入滴有酚酞试液的水中,此实验能证明上述四点性质中的(?)
A.①④
B.①②④
C.①③④
D.①②③④
参考答案:D
本题解析:K元素的原子结构与Na很相似,因此K的性质可完全类比于Na的性质,只是比Na与水的反应更剧烈。
本题难度:简单
4、选择题 把碳酸氢钠溶液滴入下列溶液中,能反应并放出气体的是(?)
A.NaOH溶液
B.石灰水
C.硫酸氢钠溶液
D.氯化铝溶液
参考答案:CD
本题解析:碳酸氢钠和氢氧化钠反应生成的是碳酸钠和水;碳酸氢钠和石灰水反应生成的是碳酸钙;硫酸氢钠能电离出氢离子,和碳酸氢钠反应生成CO2;氯化铝和碳酸氢钠水解相互促进,生成氢氧化铝和CO2,所以答案选CD。
本题难度:一般
5、选择题 下列关于碱金属元素的叙述正确的是(?)
A.它们都能在空气中燃烧生成M2O
B.它们失去电子的能力很强,故在自然界中无游离态存在
C.它们的焰色反应都是黄色
D.它们都能与水反应生成碱和氢气
参考答案:BD
本题解析:碱金属元素在空气中燃烧,Na生成了Na2O,则K、Rb、Cs都生成了比较复杂的化合物,故选项A是错的,选项B是正确的。只有Na的焰色反应才是黄色的,而其他碱金属元素的焰色反应却不是这样的,故C项是错误的。碱金属元素与水反应是剧烈的,都能生成碱和氢气,所以D项是正确的。
本题难度:简单