1、简答题 (1)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是______,在相同温度和相同压强条件下,都为气体时体积最大的是______.
(2)漂白粉的有效成分是______.
(3)请把硫酸在下列使用过程中所表现出的性质填写在空白处:
①浓硫酸常作某些气体的干燥剂:______;
②红热的炭放入浓硫酸中,有气体放出:______;
③蔗糖中加入浓硫酸时,蔗糖变黑:______.
(4)由以下一些微粒:
C、K、Ca、C、N、Ar.
互为同位素的是______和______;
(5)可用一种试剂(可加热)鉴别四种溶液NaNO3、Na2CO3、(NH4)2SO4、NH4C1,该试剂为______.
(6)要除去氯化钠里混有的少量溴化钠和碘,可先将固体混合物______,使碘______,把碘除去;再将处理过的残渣溶于水,向溶液中先______,充分反应后,再加入适量的______,分层后进行______操作,最后将溶液蒸发结晶,即得到纯净的NaCl.
(7)材料是人类赖以生存和发展的重要物质基础.住宅建设需大量的建筑材料,下列物质不属于硅酸盐材料的是______(填字母).
a.水泥b.石灰石c.玻璃.
参考答案:(1)由n=mM=VVm=NNA可知,气体的摩尔质量越大,物质的量越小,分子数越小,体积越小,质量相同的H2、NH3、SO2、O3五种气体中,SO2的摩尔质量最大,则物质的量最小,分子数最小,氢气的摩尔质量最小,则物质的量最大,体积最大;
故答案为:SO2;H2;
(2)漂白粉的有效成分是次氯酸钙;
故答案为:Ca(Cl0)2;
(3)①浓硫酸常作某些气体的干燥剂,利用了浓硫酸的吸水性,
红热的炭放入浓硫酸中,有气体放出,利用了浓硫酸的强氧化性,
蔗糖中加入浓硫酸时,蔗糖变黑,利用了浓硫酸的脱水性,
故答案为:①吸水性; ②强氧化性; ③脱水性;
(4)12C、13C是质子数相同,中子数不同的同一元素的不同原子,互称同位素;
故答案为:12C、13C;
(5)加入Ba(OH)2溶液,(NH4)2SO4生成刺激性气体和白色沉淀,NH4Cl只生成刺激性气体,Na2CO3只生成白色沉淀,NaNO3无现象,可鉴别;
故答案为:Ba(OH)2;
(6)由于碘升华,故可采用加热升华的方法除去碘单质,氯气的氧化性比溴强,可通入氯气把溴离子氧化为单质溴,溴易溶于有机溶剂,可用萃取、分液的方法分离;
故答案为:加热、升华、通入过量的氯气、苯(或四氯化碳)、分液;
(7)常见的硅酸盐材料有:水泥、玻璃和陶瓷,石灰石的主要成分是碳酸钙,不是硅酸盐材料;
故选:b;
本题解析:
本题难度:一般
2、简答题 化学兴趣小组为探究铁与浓硫酸反应,设计了如下图所示装置进行实验,回答相关问题.
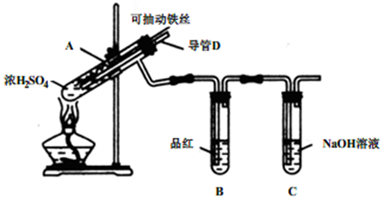
(1)用“可抽动的铁丝”代替“直接投入铁片”的优点是:______.
(2)能说明有SO2气体产生的实验现象是______.
(3)反应后,不需要打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是______.
(4)反应一段时间后,他们对A中溶液的金属离子进行探究,请完成相关问题.
①提出假设:
假设1:只含有Fe3+;
假设2:______;
假设3:既有Fe2+,又有Fe3+.
②设计实验方案验证假设3.在答题卡上写出实验步骤、预期现象和结论.
限选试剂及仪器:稀硫酸、KMnO4溶液、NaOH溶液、淀粉-KI溶液、H2O2溶液
| 实验步骤 | 预期现象和结论
步骤一:用胶头滴管取A试管中的溶液,用水稀释并分装试管I、II备用
______
步骤二:往试管I中,______
______
步骤三:______
______
参考答案:(1)在加热的条件下,当铁丝与浓硫酸接触时才能反应,当往上抽动铁丝时,铁丝与硫酸不接触,反应停止,所以用“可抽动的铁丝”的优点是便于控制反应的反应,故答案为:便于控制反应的反应和停止;
(2)SO2具有漂白性,品红能被二氧化硫漂白,可用品红溶液验证SO2的生成,所以能说明有SO2气体产生的实验现象是品红溶液褪色,故答案为:品红溶液褪色;
(3)从D管口向装置A中大量鼓气,就可使装置中残留气体完全被吹出,气体被赶到从装置BC中通过,经过B时,二氧化硫被吸收,经过C时已经完全吸收,故答案为:从D管口向A中大量鼓气;
(4)①铁与浓硫酸反应,铁可能被氧化成Fe3+或Fe2+;对A中溶液的金属离子,可能有:只含有Fe3+;只含有Fe2+;
既有Fe2+,又有Fe3+,三种情况,故答案为:只含有Fe2+;
②设计实验方案验证假设3:须验证Fe3+和Fe2+,步骤一:用胶头滴管取A试管中的溶液,用水稀释并分装试管I、II备用,二价铁离子浅绿色,三价铁离子棕黄色,所以预期现象和结论是溶液有颜色;步骤二:往试管I中,滴加少量的淀粉KI溶液,若溶液变蓝色,Fe3+能氧化碘离子,把碘离子氧化成单质碘,单质碘与淀粉作用显蓝色,则说明原溶液中含有?Fe3+;步骤三:往试管II滴加到少量的?KMnO4溶液,Fe2+能还原高锰酸根离子,若溶液褪色,则说明原溶液中含有?Fe2+,结合步骤二溶液变蓝,则假设3正确,故答案为:
实验步骤预期现象和结论步骤二:滴加少量的淀粉KI溶液若溶液变蓝色,则原溶液中含有?Fe3+步骤三:往试管II滴加到少量的?KMnO4溶液若溶液褪色(浅红),则原溶液中含有?Fe2+,结合步骤二溶液变蓝,则假设3正确
本题解析:
本题难度:一般
3、选择题 浓硫酸和2mol・L-1的稀硫酸,在实验室中敞口放置。它们的质量和放置天数的关系如下图,分析a、b曲线的变化的原因是
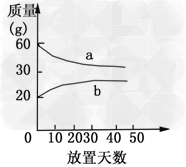
[? ]
A.a升华、b冷凝
B.a挥发、b吸水
C.a蒸发、b潮解
D.a冷凝、b吸水
参考答案:B
本题解析:
本题难度:简单
4、填空题 某高级脂肪酸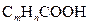 ?0.2mol完全燃烧,生成二氧化碳和水共6.8mol;同量的 ?0.2mol完全燃烧,生成二氧化碳和水共6.8mol;同量的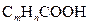 与64g溴完全加成.求该高级脂肪酸分子中m和n的值. 与64g溴完全加成.求该高级脂肪酸分子中m和n的值.
参考答案:m=17,n=31
本题解析: 为0.4mol,与0.2mol 为0.4mol,与0.2mol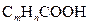 完全加成,说明该酸分子中有两个碳碳双键,则n与m的关系是:n=2m+1-4=2m-3……① 完全加成,说明该酸分子中有两个碳碳双键,则n与m的关系是:n=2m+1-4=2m-3……①
该高级脂肪酸的分子式是 ,1mol该酸完全燃烧后生成(m+1)mol ,1mol该酸完全燃烧后生成(m+1)mol 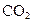 和 和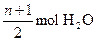 .已知0.2mol .已知0.2mol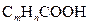 完全燃烧生成 完全燃烧生成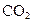 和 和 共6.8mol,则可列式:1∶〔(m+1)+ 共6.8mol,则可列式:1∶〔(m+1)+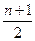 〕=0.2∶6.8 即2m+n=65……② 〕=0.2∶6.8 即2m+n=65……②
综合关系式①、②计算可得:m=17,n=31
本题难度:简单
5、选择题 分子式为CNH2NO2的羧酸和某醇酯化生成分子式为CN+2H2N+4O2的酯,反应所需羧酸和醇的质量比为1∶1,则该羧酸是
A.乙酸
B.丙酸
C.甲酸
D.乙二酸
参考答案:C
本题解析:略
本题难度:简单
|