1������� ��1���±�Ϊij�¶Ⱥ�ѹǿ�£��ܱ�������SO2����ΪSO3��Ӧ�ڲ�ͬʱ������ʵ�Ũ�ȣ�mol/L��
| ʱ�䣨min�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70
|
| SO2 | 10 | 7 | 5 | 3.5 | 2 | 1 | 1 | 1
|
| O2 | 5 | 3.5 | 2.5 | 1.75 | 1 | 0.5 | 0.5 | 0.5
|
| SO3 | 0 | 3 | 5 | 6.5 | 8 | 9 | 9 | 9
|
�Ի���V��SO3��-tͼ��
��2����ҵ����������ʱ�����ô�������Ӧ��SO2ת��ΪSO3��һ���ؼ����裮ѹǿ���¶ȶ�SO2ת���ʵ�Ӱ�����±���ԭ�������ɷֵ��������Ϊ��SO2��7%��O2��11%��N2��82%����
ѹǿ/MPa
�¶�/�� | 0.1 | 0.5 | 1 | 10
400
99.2%
99.6%
99.7%
99.9%
500
93.5%
96.9%
97.8%
99.3%
600
73.7%
85.8%
89.5%
96.4%
|
��������ñ��������ƶ�SO2��������Ӧ����ЧӦ��______��
����400һ500��ʱ��SO2�Ĵ��������ó�ѹ�����Ǹ�ѹ����Ҫԭ���ǣ�______��
�۹�ҵ��������������β������SO2������SO3��������Ϊ�˱���������β��ͨ�백ˮ�У��ܷ��������Ӧ��д�����п��ܷ���������������ԭ��Ӧ�Ļ�ѧ����ʽ��______��
�������ڲⶨ����β����SO2��������______��������ĸ��
A��NaOH��Һ����̪��Һ��?
B��KMnO4��Һ��ϡH2SO4
C����ˮ��������Һ��������
D����ˮ����̪��Һ
��ij�¶��£�SO2����ΪSO3��10L���ܱ������н��У���ʼ����������4.0mol?SO2��10.0mo1O2������Ӧ�ﵽƽ��ʱ���������Ϊ13.0mol����SO2��ת����Ϊ______�����¶ȷ�Ӧ��ƽ�ⳣ��______��
�ο��𰸣���1�����ݱ������ݷ�������������������ɵ���Ϊ0����Ӧ��50min����������Ũ�Ȳ��ٱ仯��˵���Ѵﵽƽ�⣬���ݸ�������������ϵ��������ߣ������仯������ͼ��
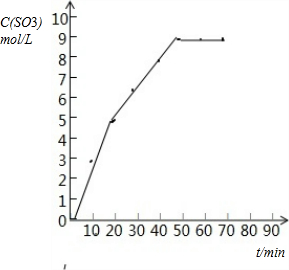
�ʴ�Ϊ��

��
��2�����������ݷ�����ѹǿһ��ʱ���¶����ߣ����������ת���ʼ�С��˵������ƽ�����淴Ӧ�����ƶ������Զ��������������ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ��ѹǿһ��ʱ���¶����ߣ����������ת���ʼ�С��˵������ƽ�����淴Ӧ�����ƶ������Զ��������������ӦΪ���ȷ�Ӧ��
��ѹǿ���¶ȶ�S02ת���ʵ�Ӱ�����ݱ������ݣ�400�桫500��ʱ��1������ѹʱ��������ת����Ϊ97.8%��99.7%��10����ѹʱ��������ת����Ϊ99.3%��99.7%���Ա����ݿ�֪������10������ѹ����������ת���ʱ仯��������ѹǿ����豸Ҫ����ߣ��ɱ��ߣ����Թ�ҵ��ֱ�Ӳ��ó�ѹ��
�ʴ�Ϊ���ӻ�ѧƽ���ƶ���������Ӧ�ò��õ��¸�ѹ�������ݱ������ṩ�����ݷ��֣�ѹǿ����������SO2ת���ʵı仯�������ԣ��������ӳɱ������Թ�ҵ��ֱ�Ӳ��ó�ѹ��
��β������S02������S03�����������ж�������ᷢ����Ӧ���������ᡢ������李���������泥���Щ�����ױ��������ʴ�Ϊ��2H2SO3+O2=2H2SO4�� 2NH4HSO3+O2=2NH4HSO4��2��NH4��2SO3+O2=2��NH4��2SO4�е�����������
�ܲⶨ����β����S02������β���к�������������Ҫ�������������Ӧ���Լ���������������Ӧ�����������ԣ�Na0H��Һ����̪��Һ�Ͱ�ˮ����̪��Һ���Ͷ���������������Ӧ�����Բ���ȷ�ⶨ��������ĺ�����KMnO4��Һ��ϡH2SO4�Ͷ�������Ӧ��ȫ����Ӧ�������ǵ���Һ�Ϻ�ɫǡ����ȥ���͵�ˮ��������Һ��Ӧ����������ȫ����Ӧ����������ɫǡ�ñ�Ϊ��ɫ������������ء��ⵥ�ʺͶ�������Ӧ������������Ӧ���������÷�Ӧ�����㱻�Լ����յĶ������õ���������ĺ������ʴ�Ϊ��BC��
�ݸ��ݶ�����������Ϊ��������ķ�Ӧ��ʽ���㣬��仯�Ķ����������ʵ���ΪX
? 2SO2 +O2 ����.��?2SO3
��ʼ����mol��?4.0? ?10.0? ?0
�仯����mol��? X? 0.5X? ?X
ƽ������mol�� 4.0-X? 10.0-0.5X? ? X
��?4.0-X?��+��10.0-0.5X?��+X=13.0?
���X=2mol
���������ת����=2mol4mol��100%=50%��k=[SO3]2[O2][SO2]2=(210)29��(210)2=1.1L?mol-1
�ʴ�Ϊ��50%��1.1L?mol-1
���������
�����Ѷȣ�һ��
2��ѡ���� ��������е�O����18O���Ҵ������е�O����16O��������һ�������·�Ӧ������������ˮ����Է���������(? )
A��16
B��18
C��20��������
D��22
�ο��𰸣�C
�������������������Ӧ�Ķϼ����ɣ��÷�Ӧ�Ļ�ѧ����ʽΪ��
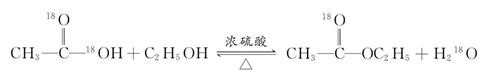
��Cѡ����ȷ��
�����Ѷȣ�һ��
3������� ��1����һ����ɫ��ΰ�Ķ�����Ѩ�зֱ����������CuSO4?5H2O���ֱ���뼸��Ũ���ᣬ�۲����ش��������⣺
Ũ����ε�����ϣ����______����ʵ������˵��Ũ�������______�ԣ�
Ũ�������CuSO4?5H2O�У�����______����ʵ������˵��Ũ�������______�ԣ�
��2��Ϊ̽��Fe3+��ת��ΪFe2+��ʵ�����ṩ�����Լ������ۡ�0.1mol?L-1FeCl3��Һ��0.1mol?L-1FeCl2��Һ��KSCN��Һ��������ˮ�������ʵ�������ʵ�����������������գ�
ȡ����______��Һ���Թ��У���������______��������ã��μ�1��2��______�������Ա仯��˵��Fe3+��ת��ΪFe2+��
�ο��𰸣���1��Ũ����ʹ���ڣ������������ˮ�ԣ�ʹ����е��л����е�H��O��ˮ����ʽ�ѳ���ֻ���º�ɫ��̼������CuSO4?5H2O�б�ף������������ˮ�ԣ��������е�ˮ���գ��ʴ�Ϊ���ڣ���ˮ����ף���ˮ��
��2����2FeCl3+Fe�T3FeCl2��������������KSCN��Һ����ɫ��֪��ȡ����FeCl3��Һ���Թ��У��������������ۣ���Ӧ���ã��μ�KSCN��Һ����������˵��Fe3+��ת��ΪFe2+���ʴ�Ϊ��FeCl3�����ۣ�KSCN��Һ��
���������
�����Ѷȣ�һ��
4��ѡ���� ̼��Ũ���Ṳ�Ȳ���������X��ͭ��Ũ���ᷴӦ����������Yͬʱͨ��ʢ������BaCl2��Һ��ϴ��ƿ�У���ͼװ�ã������й�˵����ȷ����
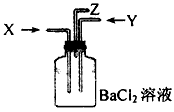
[? ]
A��ϴ��ƿ�в����ij�����̼�ᱵ
B����Z���ܳ�����������CO2
C��ϴ��ƿ�в����ij����������ᱵ
D����Z���ܿ��к���ɫ�������
�ο��𰸣�D
���������
�����Ѷȣ���
5��ѡ���� ˮ���������ȡ����ס���ʹ��Ч�����磬ˮ�����ֲ������ȡ�����ڣ�����ˮ��ȩ�ϳɡ�ˮ����Ľṹ��ʽΪ

����˵������ȷ����(? )
A��ˮ��ȩ��ȡˮ����ķ�Ӧ�Ǽӳɷ�Ӧ��Ҳ��������Ӧ
B��ˮ������������ԣ������Ȼ������ԣ������������Լ���
C��ˮ������ʹ���Ȼ�����Һ����ɫ
D��ˮ��ȩ�ܷ���������Ӧ
�ο��𰸣�AB
����������ǻ�������������ͬ��ˮ������������ǻ���û����������ѡ��B����ȷ��ˮ��������к��з��ǻ���ˮ������б��ӵ����ʣ���ʹ�Ȼ�����Һ����ɫ��ѡ��C��ȷ����ˮ����ṹ���Ƶ�ˮ��ȩ�ṹ��
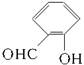
ˮ��ȩ�����к���ȩ�����ܷ���������Ӧ��Ҳ�ܷ����ӳɷ�Ӧ�����ⷴӦ�ǻ�ԭ��Ӧ������������Ӧ��ѡ��A����ѡ��D�ԡ�
�����Ѷȣ�һ��