1��ѡ���� ij����Ԫ��ԭ�ӣ���M�ܲ�����һ����������ܼ�����ԭ�ӵ�������?��?��
A��ֻ����11
B��������24
C��������29
D��������11��15
�ο��𰸣�D
���������M�ܲ�����һ����������ܼ����������3s��Ҳ������3p������������������11��Ҳ������15����ѡD��
�����Ѷȣ�һ��
2������� (8��)�±���Ԫ�����ڱ��Ķ����ڲ��֣�������ĸ�ֱ��ʾһ��Ԫ�ء���ش��������⣺
��1�� fԪ�������ڱ��е�λ���ǵ�?���ڵ�?�塣
��2�� e ��f��Ԫ������������ˮ�������Ӧ�Ļ�ѧ����ʽΪ
����?_____________________________________________________
��3��e�ڿ�����ȼ�յIJ���������ѧ��������Ϊ__________��__________��
��4�� ������ca3�ĵ���ʽΪ?��c��d����Ԫ���⻯����ȶ��Ը�ǿ���� _______�������ʵĻ�ѧʽ����
�ο��𰸣�(ÿС��2�֣���8��)
��1�� 3? IIIA? (2��)?��2��NaOH+Al(OH)3=NaAlO2+2H2O ?(2��)?
��3�� ���Ӽ������ۼ� (2��)?��4��?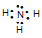 ?(1��)? H2O(1��)
?(1��)? H2O(1��)
�����������3������f��Ԫ�����ڱ��е�λ�ÿɵ��ڵ������ڡ�IIIA����2��eΪ�ƣ�����������Ӧ��ˮ����ΪNaOH��fΪ��������������Ӧ��ˮ����ΪAl(OH)3���ʷ���ʽΪ��NaOH+Al(OH)3=NaAlO2+2H2O����3�����ڿ�����ȼ�����ɹ������ƣ������Ӻ���������֮���γ����Ӽ���������������������ԭ��֮���γɹ��ۼ�����4�������ĵ���ʽע�ԭ�ӵŶԵ��ӣ�ͬ���ڴ���������̬�⻯����ȶ�������ǿ����H2O>NH3��
�����Ѷȣ�һ��
3��ѡ���� ��6�֣���2012?�㶫����ͼ�Dz��ֶ�����Ԫ�ػ��ϼ���ԭ�������Ĺ�ϵͼ������˵����ȷ���ǣ�������

A��ԭ�Ӱ뾶��Z��Y��X
B����̬�⻯����ȶ��ԣ�R��W
C��WX3��ˮ��Ӧ�γɵĻ����������ӻ�����
D��Y��Z��������������Ӧ��ˮ���������Ӧ
�ο��𰸣�BD
���������Ϊ������Ԫ�أ�������Ԫ�ؼ���+4�ۣ����Щ�4�ۣ���ǰһ��Ԫ��Ϊ̼����һ��Ԫ��Ϊ�裬��RΪSiԪ�أ�X�Ļ��ϼ�Ϊ��2�ۣ�û�������ϼۣ���XΪOԪ�أ�Y�Ļ��ϼ�Ϊ+1�ۣ����ڢ�A�壬ԭ����������OԪ�أ���YΪNaԪ�أ�ZΪ+3�ۣ�ΪAlԪ�أ�W�Ļ��ϼ�Ϊ+6����2�ۣ���WΪSԪ�أ�
�⣺Ϊ������Ԫ�أ�������Ԫ�ؼ���+4�ۣ����Щ�4�ۣ���ǰһ��Ԫ��Ϊ̼����һ��Ԫ��Ϊ�裬��RΪSiԪ�أ�X�Ļ��ϼ�Ϊ��2�ۣ�û�������ϼۣ���XΪOԪ�أ�Y�Ļ��ϼ�Ϊ+1�ۣ����ڢ�A�壬ԭ����������OԪ�أ���YΪNaԪ�أ�ZΪ+3�ۣ�ΪAlԪ�أ�W�Ļ��ϼ�Ϊ+6����2�ۣ���WΪSԪ�أ�
A��ͬ������ԭ����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����ԭ�Ӱ뾶Na��Al��O����Y��Z��X����A����
B����Ȼ�ǽ�����S��Si����SiH4�ķֽ��¶ȱ�H2S�ߣ����ȶ�����B��ȷ��
C��SO3��H2O��������H2SO4��H2SO4�ǹ��ۻ������C����
D��NaOH��Al��OH��3�ܷ�����Ӧ��NaOH+Al��OH��3=NaAlO2+2H2O����D��ȷ��
��ѡBD��
���������⿼��ṹ������λ�ù�ϵ��Ԫ�������ɵȣ��ѶȲ������ƶ�Ԫ���ǽ���Ĺؼ������ݻ��ϼ۽��ԭ�����������ƶϣ�����������Ҫץס��������Ԫ�ء������֣�
�����Ѷȣ�һ��
4��ѡ���� ����˵����ȷ����(? )
A��ԭ�Ӻ˶��������Ӻ����ӹ��ɵ�
B����ͬԪ��ԭ�ӵ�������һ������
C������������Ԫ�����࣬������������������ԭ������
D����������ͬ�����ӣ�����������һ����ͬ������ѧ���ʲ�һ����ͬ
�ο��𰸣�C
���������Hԭ���в��������ӣ�A����ȷ����ͬԪ��ԭ�ӵ��������п�����ȣ�B����ȷ��������ͬ�˵��������������ͬһ��ԭ�ӵ��ܳ���Ԫ�أ�������������Ԫ�����ࡣ����һ����Ŀ���Ӻ�һ����Ŀ���ӵ�һ��ԭ���Ǻ��أ����������������������ԭ�����࣬C��ȷ����������ͬ�����ӣ�������������һ����ͬ����ѧ���ʲ�һ����ͬ��������ԭ�Ӻ������ӣ�D����ȷ����ѡC��
�����������Ǹ߿��еij������ͺͿ��㣬�����е��Ѷȵ����⡣�����ۺ���ǿ�����ض�ѧ������������������Ĺؼ���ѧ��ͨ�������ų���һɸѡ�ó���ȷ���۵Ľ��ⷽ����������ͨ��ѧ����Ӧ��������ѧϰЧ�ʡ�
�����Ѷȣ�һ��
5��ѡ���� ������ͬλ���ص�������A=166��������Z=67��������������������֮��Ϊ
A��166
B��67
C��99
D��32
�ο��𰸣�D
�������������ԭ�ӵ���ɼ���ʾ�������ڱ�ʾԭ�����ʱԪ�ط��ŵ����½DZ�ʾ�����������ϽDZ�ʾ����������Ϊ��������������֮�����������������������ں������������������������������֮��Ϊ166��67��67��32����ѡD��
�����Ѷȣ���