1、填空题 (10分)铅蓄电池是化学电源,其电极材料分别是Pb和PbO2,电解质溶液为稀硫酸。工作时,该电池的总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O根据上述情况判断:
(1)蓄电池的负极是______,其电极反应式为______。
(2)蓄电池的正极是______,其电极反应式为______。
(3)蓄电池工作时,其中电解质溶液的pH______(增大、减小、不变)。
(4)实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得Cl2?0.050mol,这时电池内消耗的H2SO4的物质的量至少是?。
参考答案:
(1)Pb? Pb - 2e- +SO42-=PbSO4?
(2)PbO2?PbO2 + 4H++SO4 +2e-=? PbSO4?+ 2H2O
(3)增大
(4)1mol
本题解析:由总反应中的元素化合价的升降可知
Pb在负极失电子:Pb - 2e- +SO42-=PbSO4
PbO2在正极得电子:PbO2 + 4H++SO4 +2e-=PbSO4 + 2H2O
电池工作过程中,消耗硫酸,电解质溶液的酸性减弱,pH增大
(4)电解食盐水:2NaCl+2H2O=2NaOH+H2↑+Cl2↑,当制得0.050mol氯气时,电路中电子的转移为0.1mol,而在电池内部(反应中有两个电子转移),必定耗硫酸最少0.1mol
本题难度:简单
2、选择题 镁燃料电池以镁合金作为电池的一极,另一极充入过氧化氢,电解质溶液是酸化的氯化钠溶液,放电时总反应:Mg+2H++H2O2= Mg2++2H2O。关于该电池说法正确的是
A.镁合金为电源负极,发生氧化反应
B.放电时H+在正极反应得电子
C.正极方程式为:H2O2+2e-=2OH-
D.放电时正极的pH降低
参考答案:A
本题解析:(―)Mg―2e―= Mg2+;(+)H2O2+2e―+2H+=2H2O,得到电子的是H2O2,判断B错有点难。
本题难度:一般
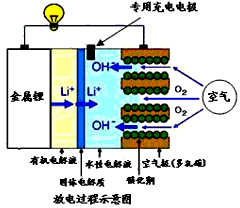
3、选择题 最近研发了一种新型的锂空气电池,它既可用作充电电池又可作锂燃料电池。用作燃料电池时,可更换正极的水性电解液和卡盒以及负极的金属锂就可以连续使用,分离出的氢氧化锂可采用电解其熔融物法回收锂而循环使用。下列叙述不正确的是
[? ]
A.充电时,阳极的电极反应式为:2H2O+O2+4e-=4OH-
B.放电时负极的电极反应式为:Li-e- = Li+
C.充电时,锂极与外电源的负极相连
D.熔融的氢氧化锂用惰性电极电解再生时,金属锂在阴极得到
参考答案:A
本题解析:
本题难度:一般
4、选择题 氢氧燃料电池以H2为还原剂,O2为氧化剂,电极为多孔镍,电解液为30%的KOH溶液,下列有关叙述正确的是
[? ]
①负极质量减轻 ②负极反应为4OH--4e-=O2↑+2H2O ③负极反应为H2+2OH--2e-=2H2O
④工作时正极区pH升高,负极区pH降低?⑤工作时溶液中阴离子移向正极?
A.①③④
B.②③⑤
C.④⑤
D.③④
参考答案:D
本题解析:
本题难度:一般
5、选择题 锂钒氧化物电池的能量密度远远超过其他材料电池,电池总反应式为:V2O5+xLi→LixV2O5,下列说法不正确的是
A.向外供电时,锂离子向负极移动
B.负极上反应的物质是锂,正极上反应的物质是V2O5
C.正极的电极反应为:V2O5+xe-+xLi+→LixV2O5
D.负极的电极反应为:xLi-xe-→ xLi+
参考答案:A
本题解析:反应中V由+5价降为 价,Li由0价升为+1价,负极上反应的物质是Li,正极上反应的物质是V2O5,B正确;负极反应为Li-e-=Li+,D正确;正极反应为V2O5+xe-+xLi+=LixV2O5,C正确;原电池内部阳离子向正极迁移、阴离子向负极迁移,A错误。
价,Li由0价升为+1价,负极上反应的物质是Li,正极上反应的物质是V2O5,B正确;负极反应为Li-e-=Li+,D正确;正极反应为V2O5+xe-+xLi+=LixV2O5,C正确;原电池内部阳离子向正极迁移、阴离子向负极迁移,A错误。
点评:原电池中负极失电子、正极得电子;原电池内部阳离子向正极迁移、阴离子向负极迁移。
本题难度:简单