1、选择题 将Mg、Cu组成的2.64 g混合物投入到100 mL稀硝酸中完全溶解,并收集还原产物NO气体(还原产物只有一种)。然后向反应后的溶液中逐滴加入2 mol・L-1 NaOH溶液,下图是生成沉淀的质量与滴入NaOH溶液体积间的关系图。以下说法不正确的是
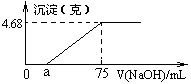
[? ]
A.稀硝酸的浓度为1.9 mol/L
B.生成的NO在标况下的体积为0.896 L
C.a的值为15 mL
D.Cu的物质的量为0.02 mol
参考答案:D
本题解析:
本题难度:一般
2、填空题 胃酸过多是常见的胃病。下面是甲、乙两种常见胃药的说明摘要。
甲:①白色结晶状粉末,受热可缓缓分解;
②能溶于水,水溶液呈弱碱性;灼烧时火焰为黄色;
③遇酸及酸性药物则产生二氧化碳;
④患者服用过量,可能引起胃胀气,甚至有引起胃溃疡穿孔的危险。
乙:①与胃酸是中和作用缓慢而持久,可维持3~4小时;
②凝胶本身覆盖于溃疡面上,具有保护作用;
③可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成份是____________(填化学式);乙中含有的主要化学成份是
____________(填化学式)。
(2)试写出甲中含有的主要化学成份引起胃胀气反应的离子方程式:____________________________。
(3)三硅酸镁Mg2Si3O8・nH2O也是常用胃药,被用来治疗胃溃疡,是因为该物质不溶于水,服用后中和胃酸作用持久。把三硅酸镁改写成氧化物形式为:_________________________。写出它中和胃酸(胃酸的主要成分是HCl)的化学方程式_______________________________。
(4)目前一种新型抗酸剂能迅速改善和缓解胃酸过多的症状,它主要由碳酸镁、氢氧化镁和氢氧化铝组成(说明:Mg(OH)2在高温下分解为MgO)。现按如下步骤测定药剂中三种主要成分的配比:
①取药剂样品,研磨后,加入50mL3.6 mol・L-1盐酸,正好完全反应并收集得到标准状况下224mL气体
②过滤,弃去其中不溶性物质(其余成分不参与反应)
③取②中滤液,加入足量的NaOH溶液后,过滤、洗涤、灼烧,所得固体2.4g。
则该药剂中三种主要成分的物质的量之比为n(MgCO3):n(Mg(OH)2):n(Al(OH)3)=_________。
参考答案:(1)NaHCO3; Al(OH)3
(2)HCO3-+H+==H2O+CO2↑
(3)2MgO・3SiO2・nH2O;Mg2Si3O8・nH2O+4HCl==2MgCl2+3H2SiO3↓+(n-1)H2O
(4)n(MgCO3):n(Mg(OH)2):n(Al(OH)3)=1∶5∶2
本题解析:
本题难度:一般
3、选择题 往含0.2mol?NaOH和0.1mol?Ca(OH)2的溶液中持续稳定地通入CO2气体,当通入气体的体积为6.72L(标准状况下)时立即停止,则在这一过程中,溶液中离子数目和通入CO2气体的体积关系正确的图像是(气体的溶解忽略不计)?
[? ]
A.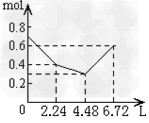
B.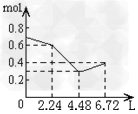
C.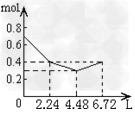
D.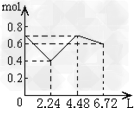
参考答案:C
本题解析:
本题难度:一般
4、选择题 常温下,某同学向100 mL H2S饱和溶液中通入SO2,所得溶液pH与加入气体体积(标况下的数据)变化如图所示。下列分析中,正确的是
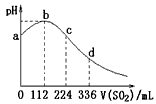
[? ]
A.b 点所对应的纵坐标数据为7
B.亚硫酸是比氢硫酸更弱的酸
C.原H2S溶液的物质的量浓度为0.05 mol/L
D.b 点对应的溶液导电性最强
参考答案:A
本题解析:
本题难度:一般
5、计算题 有一铝、镁、硅组成的合金,取5.3g合金与足量的盐酸反应,结果残余固体有0.2g ,收集到气体体积5.6L(已换算到标准状况),求此合金中铝、镁的物质的量?
参考答案:0.1 mol、0.1 mol
本题解析:
本题难度:一般