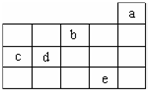
1������� A��B��C��D��E���ֶ�����Ԫ�أ����ǵĺ˵������C��A��B��D��E˳����������C��D���ֱܷ���A��ԭ�Ӹ�����Ϊ1��1��2��1�γɻ����CB��ˮ��Һ���ܷ��ڲ��������У�A��E���γɻ�ѧʽΪEA2��EA3���ֻ�������Ƕ�����D������������ˮ���ﷴӦ��
��1��D�����ڱ��е�λ��Ϊ______��
��2��C��A�γɵĻ������У����м��Լ����зǼ��Լ��Ļ�����Ļ�ѧʽΪ______��
��3��д��E����̬�⻯��������D������������ˮ���ﷴӦ�����ӷ���ʽ______��
��4��������Ԫ���У�ѡ����ͬԪ��������ֻ�����X��Y��
�������X��Y��ˮ��Һ�ܷ�����Ӧ��д�����ӷ���ʽ______��
����X�ʼ��ԣ��ڿ����о��û���Y��д��X�Ļ�ѧʽ______��
��X�����ԣ��ڿ����о��û���Y��д��X������______
��5��DC��C2A��Ӧ�Ļ�ѧ����Ϊ______��
�ο��𰸣�������Ԫ�أ��˵������C��A��B��D��E˳����������C��D���ֱܷ���A��ԭ�Ӹ�����Ϊ1��1��2��1�γɻ������CΪH��AΪO��DΪNa��CB��ˮ��Һ���ܷ��ڲ��������У���CBΪHF������BΪF��A��E���γɻ�ѧʽΪEA2��EA3���ֻ�������Ƕ�����D������������ˮ���ﷴӦ����E��+4��+6�ۣ�����EΪS��
��1��DΪNa��ԭ������Ϊ11��ԭ�ӽṹ����3�����Ӳ㣬����������Ϊ1����λ��Ԫ�����ڱ��е�������IA�壬
�ʴ�Ϊ����������IA�壻
��2��C��A�γɵĻ�������H2O��H2O2����ˮ��ֻ�м��Լ���H2O2�м��м��Լ���H-O�������зǼ��Լ���O-O����
�ʴ�Ϊ��H2O2��
��3��E����̬�⻯��ΪH2S����Һ�����ԣ������кͷ�Ӧ��D������������ˮ����ΪNaOH��������ʱ�����ӷ�ӦΪ
H2S+OH-�THS-+H2O���ʴ�Ϊ��H2S+OH-�THS-+H2O��
��4����ѡ��Na��H��O��SԪ�أ����������������������Ʒ�Ӧ���������ơ����������ˮ��
���ӷ�ӦΪH++HSO32-�TSO2+H2O���ʴ�Ϊ��H++HSO32-�TSO2+H2O��
������������Һ�Լ��ԣ������������ױ��������������ƵĻ�ѧʽΪNa2SO3����������Ϊ�ᣬ�ױ�����Ϊ���ᣬ
�ʴ�Ϊ��Na2SO3�������
��5��NaH��HԪ��Ϊ-1�ۣ�ˮ��HԪ��Ϊ+1�ۣ����߷���������ԭ��Ӧ���÷�ӦΪNaH+H2O�TH2+NaOH��
�ʴ�Ϊ��NaH+H2O�TH2+NaOH��
���������
�����Ѷȣ�һ��
2��ѡ���� 2009��������8�յ磬��aa2���й���ѧԺԺʿ���й�����ԺԺʿͶƱ��ѡ����2008������ʮ��Ƽ���չ���Ž��������������������о����ش��չ�����а����ձ����й���ѧ����̷��ֵ��µĸ��³�������--�����������ϣ���ɷ��Ƿ������磨La�������飨As������������йظò��ϵ��ж���ȷ���ǣ�������
A�������ڱ��У��ò�����������Ԫ��������λ�����壬����λ�ڸ���
B���ó���������������Ԫ�������ֽ���Ԫ�أ����ַǽ���Ԫ��
C���ó�����������ḯʴ
D�������ڱ��У���λ�ڵ�VIII�壬��λ�ڵ�������
�ο��𰸣�q�������ʺ��з������������顢������Ԫ�أ�F��O��qsΪ����Ԫ�أ����ò�����������Ԫ��������λ�ڸ��壬����λ�����壬��q����
B�������ʺ��з������������顢������Ԫ�أ�������Ϊ����Ԫ�أ���������������Ԫ�������ֽ���Ԫ�أ����ַǽ���Ԫ�أ���B��ȷ��
C������Ϣ��֪���ò���Ϊ��6���³������ϣ�������С6Fe���ᷴӦ���������ḯʴ����C����
D�������ڱ�С����λ�ڵ������ڵ�VIII�壬��λ�ڵ������ڵڢ�q�壬��D��ȷ��
��ѡBD��
���������
�����Ѷȣ���
3��ѡ���� �������ʵĻ�ѧ������ȷ����
[? ]
��NH4H�ĵ���ʽ�� ���������Ľṹ��ʽ��
���������Ľṹ��ʽ��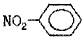
�������ǵ�ʵ��ʽ��CH2O �ܼ�����ӵı���ģ�ͣ�
��Fe2+�����ӽṹ��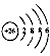 ��sp2�ӻ����ģ�ͣ�
��sp2�ӻ����ģ�ͣ�
��ԭ�Ӻ�����10�����ӵ���ԭ�ӣ�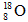
A���ڢۢޢ�
B���٢ۢݢ�
C���ۢޢ�
D���٢ڢۢܢݢޢ�
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� ����������ӣ������ȶ�������ˮ�⣬�ڸߵ�ѹ���������õľ�Ե�ԣ��ڵ�����ҵ���Ź㷺��;������ɢ�������л�����ǿ����ЧӦ�������й�SF6���Ʋ���ȷ����
A��SF6��ȼ�����ɶ�������
B��SF6�и�ԭ�Ӿ��ﵽ 8 �����ȶ��ṹ
C���۲���Ӷ���Ϊ6����������ṹ
D��SF6���ɼ��Լ����ɵķǼ��Է���
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
5��ѡ���� ͼΪ���ڱ�ǰ4���ڵ�һ���֣����й���a��b��c��d��e��������ȷ���ǣ�������
A��bԪ�س�0���⣬ֻ��һ�ֻ��ϼ�
B������Ԫ���У�cԪ���γɵĵ����������ȶ�
C��c��dԪ������������ˮ�������ԣ�c��d
D��eԪ������Ȼ������Ҫ�����ں�ˮ��