1、选择题 设NA表示阿伏加德罗常数的值。下列叙述不正确的是
A.1 mol Na2O和Na2O2的混合物中含有的阴、阳离子总数是3NA
B.常温下,1 L 0.1 mol・L-1的NH4NO3溶液中含有的氮原子数为0.2NA
C.46 g有机物C2H6O中含有的H―O键的数目为NA
D.标准状况下,将0.1 mol Cl2通入足量NaOH溶液中,反应转移的电子数为0.1NA
参考答案:C
本题解析: A、氧化钠和过氧化钠中阴、阳离子个数比均为1:2,正确;B、由物料守恒可知含0.1molNH4NO3的溶液中N原子总数为0.2mol,正确;C2H6O可表示乙醇或二甲醚,若表示二甲醚,则其中不存在H-O键,错误;D、氯气与氢氧化钠溶液反应时,氯气既是氧化剂又是还原剂,正确。A
本题难度:一般
2、选择题 CaCl2溶解在1mol H2O中,使Cl―与H2O分子的物质的量之比为1:10时,CaCl2为(? )
A.0.1mol
B.10mol
C.0.5mol
D.0.05mol
参考答案:D
本题解析:1molH2O中Cl-与H2O分子的物质的量之比为1:10,则Cl-的物质的量=1/10=0.1mol,1molCaCl2溶解电离出2molCl-,故需要CaCl2的物质的量=0.1/2=0.05mol,故选D。
本题难度:一般
3、选择题 设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,1.12LCCl4含有C-Cl键数目为0.2NA
B.标准状况下,2.24L氯气中含有的 Cl数目一定为0.2NA
Cl数目一定为0.2NA
C.常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA
D.80mL 10mol・L-1盐酸与足量MnO2加热反应,产生Cl2分子数为0.2NA
参考答案:C
本题解析:A、CCl4为液态,不能用气体摩尔体积计算,错误;B、天然的氯元素有2种同位素,其总量为0.2NA,错误;C、CO2与N2O摩尔质量相同,分子中原子个数相同,故原子个数为4.4÷44×3=0.3mol,正确;D、该反应中盐酸为浓盐酸,随反应进行盐酸浓度降低不再反应,故产生的Cl2分子数小于0.2NA,错误。
本题难度:一般
4、选择题 a mol Na2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为( )
A.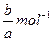
B.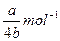
C.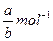
D.
参考答案:D
本题解析:略
本题难度:简单
5、计算题 已知一个氧原子的质量为2.657×10-26kg,则多少克氧气的物质的量为1mol?(要求根据氧原子的质量进行推算)
参考答案:32g
本题解析:因为1个氧分子含2个氧原子,1 mol O2约含6.02×1023个氧分子,所以有:2.657×10-26kg×2×6.02×1023=31.99×10-3kg="32.0" g。
本题难度:简单