1������� ����ѧ��Ӧ�����Dz����������ʱ仯�������仯����ͨ��Ҫ�о���ѧ��Ӧ�Ŀ���

(1)�ô�����п�������ᷴӦ��ȡ�������ش�
ʵ���������ͼ��ʾ�������жϣ�________�λ�ѧ��Ӧ������죬ԭ����?��_______���ռ���������ࡣ
Ϊ�˼ӿ�������Ӧ�����ʣ�������Һ�м���һ�����������ʣ�����Ϊ���е���?
A.��������? B.�������ƹ���
C.�Ȼ�пŨ��Һ? D.Ũ����
�������������⣬����Ϊ�����Բ�ȡ?��ʩ���ӿ컯ѧ��Ӧ���ʡ�
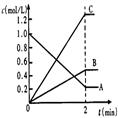
(2)��ͼ��ʾ800��ʱ��A��B��C�����������ʵ�Ũ����ʱ��仯�������t�Ǵﵽƽ��״̬��ʱ�䡣
�Իش�
�ٸ÷�Ӧ�Ļ�ѧ����ʽΪ_________________________________��
�ڴﵽƽ��״̬������ʱ����2min��A���ʵ�ƽ����ѧ��Ӧ����Ϊ______?______
�ο��𰸣���1��EF����Ӧ����,��Һ�¶�����,��Ӧ���ʼӿ죻EF��AB�����Ȼ��п������С������ʩ���ӿ컯ѧ��Ӧ����
��2����2A B+3C?��0.4mol/(L��min)
B+3C?��0.4mol/(L��min)
�����������1����Ӧ����Խ�죬�����ߵ�б��Խ�����Ը���ͼ���֪��EF�η�Ӧ������졣�������ڷ�Ӧ���ȣ���Һ�¶�����,��Ӧ���ʼӿ죻����������ı仯��֪��EF �β�����������ࣻ��������ˮ��п���û���ͭ���Ӷ�����ͭпԭ��أ��ӿ췴Ӧ���ʣ�A��ȷ��������������ˮ����������ӣ�����������Ũ�ȣ���Ӧ���ʼӿ죬B��ȷ���Ȼ�п��Ũ��Һ���ܸı������ӵ�Ũ�ȣ���Ӧ���ʱ仯����C�����������������ᣬ��п��Ӧ�ò���������D����ȷ����ѡAB�������¶Ⱥ���ı����Ҳ���Ըı䷴Ӧ���ʣ����Լ��Ȼ��п������С������ʩ���ӿ컯ѧ��Ӧ���ʡ�
��2���ٸ���ͼ���֪����Ӧ���е�2minʱ���ʵ�Ũ�Ȳ��ٷ����仯����Ӧ�ﵽƽ��״̬������A��Ũ�ȼ�����0.8mol/L��B��C��Ũ�ȷֱ�������0.4mol/L��1.2mol/L������ݱ仯��֮���ǻ�ѧ������֮�ȿ�֪���÷�Ӧ�ķ���ʽ��2A B+3C��
B+3C��
��ƽ��ʱA�ķ�Ӧ������0.8mol/L��2min��0.4 mol/(L��min)��
�����������Ǹ߿��еij������ͣ����ڻ���������Ŀ��顣���������ǿ�����ض�ѧ������֪ʶ��ѵ��������������ѧ��������û���֪ʶ���ʵ����������������ѧϰЧ�ʡ�����Ĺؼ�����ȷ��Ӧ���ʵĺ���ͱ���ʽ��Ȼ��������������ü��ɡ�
�����Ѷȣ�һ��
2��ѡ���� �ϳɰ���Ӧ��

 ���䷴Ӧ���ʿ��Էֱ���
���䷴Ӧ���ʿ��Էֱ��� ��ʾ������ȷ��ϵ��
��ʾ������ȷ��ϵ��
A��
B��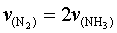
C��
D��
�ο��𰸣�C
���������
�Ժϳɰ���Ӧ����ֱ��õ�λʱ����H2��N2��NH3�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ����Ӧ�����ϵʽ��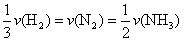 ����
���� �����ɴ˿��Ƶ��йع�ϵʽ��
�����ɴ˿��Ƶ��йع�ϵʽ��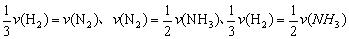 ������ȷѡ��ΪC��
������ȷѡ��ΪC��
�����Ѷȣ���
3��ѡ���� �ס������������ڶ�����A��B�ķ�Ӧ����������ÿ���Ӽ�����4molA����������ÿ���Ӽ���2molA����������ڵķ�Ӧ���ʱ��������ڵķ�Ӧ���ʣ�������
A����
B����
C�����
D�����ж�
�ο��𰸣�v=��nV��t�У���n����t��֪����Vδ֪���������жϼס��������ڵĻ�ѧ��Ӧ���ʣ�
��ѡD��
���������
�����Ѷȣ�һ��
4��ѡ���� ��Ӧ��2A+B�T2E����һ��ʱ���E��Ũ��������0.4mol/L�������ʱ������E��ʾ�ķ�Ӧ����Ϊ0.04mol/��L��S���������ʱ��Ϊ��������
A��2S
B��2.5S
C��5S
D��10S
�ο��𰸣�E��Ũ��������0.4mol/L�����ԡ�c��E��=0.4mol/L��
���ʱ������E��ʾ�ķ�Ӧ����Ϊ0.04mol/��L��S����
����t=0.4mol/L0.04mol/(L��S)=10s��
������ʱ��Ϊ10s��
��ѡ��D��
���������
�����Ѷȣ���
5��ѡ���� �����ĸ��Թ��У���������ֽ���������ķ�Ӧ������������
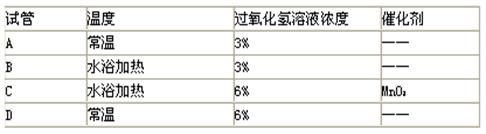
�ο��𰸣�A
�����������
�����Ѷȣ���