1、选择题 下列说法正确的是( )
A.短周期元素形成离子后,最外层均达8电子稳定结构
B.多电子原子中,在离核较近的区域运动的电子能量较低
C.非金属元素组成的化合物中只有共价键
D.HF、HCl、HBr、HI的热稳定性和还原性依次增强
参考答案:A.氢离子没有电子,不满足8电子稳定结构,故A错误;
B.离核较近的区域能量较低,能力越高的电子在离核远的区域运动,故B正确;
C.铵盐属于离子化合物,故C错误;
D.同主族自上而下非金属性减弱,非金属性越强,氢化物越稳定,还原性越强,故HF、HCl、HBr、HI的热稳定性减弱,还原性依次增强,故D错误;
故选B.
本题解析:
本题难度:简单
2、填空题 请回答下面问题
(1)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表
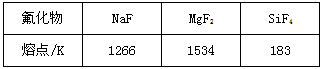
|
解释表中氟化物熔点差异的原因:____________________________________
(2)CO的结构可表示为C≡O,N2的结构可表示为N≡N。下表是两者的键能数据:(单位:kJ・mol-1)

CO与N2的结构相似,分子中都含有共价三键,其中含有___________个π键;结合数据说明CO比N2活泼的原因:____________________________________
参考答案:(1)NaF、MgF2为离子晶体,SiF4为分子晶体,所以NaF、MgF2的熔点远比SiF4熔点要高,又因为Mg2+
半径小于Na+的半径,所以MgF2的离子键强度大于NaF的离子键强度,故MgF2的熔点大于NaF的熔点。
(2)2;打开CO的第一个化学键所需的能量:1071.9-798.9=273kJ/mol,打开N2的第一个化学键所需的能量:941.7-418.4=523.3kJ/mol,前者所需的能量小,故CO更活泼
本题解析:
本题难度:一般
3、选择题 下列说法正确的是
[? ]
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.所有金属与所有非金属之间都能形成离子键
C.在化合物CaCl2中,两个氯离子之间也存在离子键
D.含有离子键的化合物一定是离子化合物
参考答案:D
本题解析:
本题难度:简单
4、选择题 在KMnO4中,Mn的化合价是( ? )
A.+2
B.+4
C.+6
D.+7
参考答案:D
本题解析:
本题难度:简单
5、填空题 (18分)下表中a、b、c…为周期表中部分元素,回答下列问
a
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| f
| y
| h
| i
| ?
|
?
| b
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| e
| ?
| ?
| ?
| j
| ?
|
c
| ?
| ?
| ?
| ?
| ?
| ?
| d
| ?
| ?
| ?
| g
| ?
| l
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
(1)在表中用线画出元素周期表的边界
(2)请写出上述元素d3+的核外电子排布式?;
(3)请比较y、h、i三种元素的第一电离能由大到小的顺序?(写元素符号),判断依据是:?
(4)请写出e元素的原子价电子轨道表示式?;
(5)ya3分子的电子式是??,其分子的空间构型是??。
(6)e元素最高价氧化物对应的水化物呈_______性(酸性、碱性或两性),用离子方程式说明____________________________________________?。
参考答案:
a
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
f
y
h
i
?
?
b
?
?
?
?
?
?
?
?
?
?
e
?
?
?
j
?
c
?
?
?
?
?
?
d
?
?
?
g
?
l
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
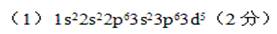
 ?两性:(2分)略
?两性:(2分)略
本题解析:(1)从图中可知,该表格有七行,即表示七个周期;有18列,即表示18个族。所以可以确定其边界应如图:
(2)从d的位置可知其为第四周期第8副族的元素,即铁元素。其原子的电子排布式应为:1s22s22p63s23p63d64s2。铁原子失去最外层的两个电子4s2时就是亚铁离子,在失去3d6中的一个电子,使d亚层达到半满状态。所以d3+的核外电子排布式为:1s22s22p63s23p63d5或[Ar]3d5
(3)从图中可知,y、h、i分别为F、N、O三种元素。
同一周期内元素的第一电离能在总体增大的趋势中有些曲折。当外围电子在能量相等的轨道上形成全空(p0, d0, fo)、半满(p3, d5, f7)或全满(p6, d10, f14)结构时,原子的能量较低,元素的第一电离能较大。所以三种元素的第一电离能由大到小的顺序为:F>N>O
(4)从图中可知:e元素为铝元素,其核外电子排布式为:1s22s22p63s23p1。所以其原子电子轨道表示式: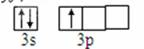
(5)根据元素周期表可知ya3应为NH3。所以其分子的电子式是:
NH3分子的空间构型是:三角锥,中心原子N原子采取SP3杂化
(6)e元素为铝元素,其最高价氧化物对应的水化物为Al(OH)3,属于两性氢氧化物,离子方程式为:Al(OH)3+OH-=AlO2- +2H2O
本题难度:一般