1、选择题 下列说法中正确的是?
A.标准状况下,22.4L水中所含的分子数约为6.02×1023
B.标准状况下,aL的氧气和氮气的混合物含有的分子数约为×6.02×1023
C.22 g二氧化碳与标准状况下11.2 L氯化氢气体含有的分子数不同
D.2.24L CO2中含有的原子数为0.3×6.02×1023
参考答案:B
本题解析:略
本题难度:简单
2、填空题 同温同压下,同体积的NH3和H2S气体的质量之比为 ____?;同质量的氨气和硫化氢气体的体积之比为? ___?;若二者氢原子数相等,则它的体积之比为? __??。
参考答案:1:2? 2:1? 2:3
本题解析:略
本题难度:简单
3、选择题 标准状况下有①6.72LCH4②3.01×1023个HCl③13.6gH2S④0.2molNH3,下列对四种气体的关系从小到大表示不正确的是
A.体积 ④<①<③<②
B.密度 ①<④<③<②
C.质量 ④<①<③<②
D.氢原子数 ④<②<③<①
参考答案:D
本题解析:根据题意可知,甲烷、氯化氢、H2S的物质的量分别是6.72L÷22.4L/mol=0.3mol、 、13.6g÷34g/mol=0.4mol。根据阿伏加德罗定律可知,气体的体积大小关系是④<①<③<②,A正确;在相同条件下,气体的密度之比是相对分子质量之比,B正确;甲烷的质量是4.8g、氯化氢的质量是18.25g、氨气的质量是3.4g,所以质量关系是④<①<③<②,C正确。氢原子的物质的量分别是1.2mol、0.5mol、0.8mol、0.6mol,则氢原子数 ②<④<③<①,D不正确,答案选D。
、13.6g÷34g/mol=0.4mol。根据阿伏加德罗定律可知,气体的体积大小关系是④<①<③<②,A正确;在相同条件下,气体的密度之比是相对分子质量之比,B正确;甲烷的质量是4.8g、氯化氢的质量是18.25g、氨气的质量是3.4g,所以质量关系是④<①<③<②,C正确。氢原子的物质的量分别是1.2mol、0.5mol、0.8mol、0.6mol,则氢原子数 ②<④<③<①,D不正确,答案选D。
点评:该题是中等难度的试题,试题综合性强,在注重对基础知识考查的同时,更侧重对学生能力的培养。该题学生需要注意的是在进行物质的量的有关计算时,关键是熟练应用几个关系式 、n=m/M、
、n=m/M、 、
、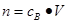 ,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。
,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。
本题难度:简单
4、选择题 阿伏加德罗常数约为6.02×1023,下列叙述正确的是(?)
A.2.24LCO2中含有的原子数为0.3×6.02×1023
B.0.1L 3 mol/L NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023
C.5.6g铁粉与硝酸反应失去电子数一定为0.3×6.02×1023
D.4.5 g二氧化硅晶体中含有的硅氧键数目为0.3×6.02×1023
参考答案:D
本题解析:A项中未指明温度、压强,无法确定N2的物质的量,A错误;由于在水溶液中NH4+离子要水解,故NH4+离子数应小于0.3NA,B错误;铁粉与硝酸反应到底生成Fe3+还是Fe2+还是Fe3+和Fe2+的混合物,不能确定,故失去的电子数不能确定,C错误;由于1 molSiO2晶体中含4 molSi―O键,故4.5 g二氧化硅晶体中含有的硅氧键数目为
(4.5g /60 g・mol-1)×4×6.02×1023=0.3×6.02×1023,D正确。故本题应选D。
本题难度:简单
5、选择题 下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板?(其质量可忽略不计)。其中能表示等质量的氢气与氦气的是
[? ]
A.
B.
C.
D.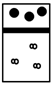
参考答案:A
本题解析:
本题难度:简单