1、填空题 (12分)根据下图所示的关系,确定A、B、C、D、E、F的化学式,并写有关方程式。

(1)已知A为单质,则A为 (填化学式,下同),E为 。
(2)D→E的化学方程式为___________________________________。
(3)取少量C溶于水,加入酸化的硝酸银溶液,有白 色沉淀生成,则A→C的化学方程式为_____________________________。
(4)某学习小组设计如下装置进行相关实验:

①打开活塞b,向溶液B中逐滴加入少量溴水,关闭活塞b;
②打开活塞a,向容器中滴入足量的亚硫酸。
按要求回答下列问题:
①滴入溴水时,溶液的颜色变为棕黄色,该反应的离子方程式为________。
②滴入亚硫酸时,溶液由棕黄色变为浅绿色,该反应的离子方程式为______。
③由此可知,B中的阳离子、Br-、H2SO3还原性由强到弱的顺序是___________(B中的阳离子用离子符号表示)。
参考答案:(1)Fe,Fe(OH)3 (2)4Fe(OH) 2+O2+2H2O=4Fe(OH)3 (3)2Fe+3Cl2 2FeCl3
2FeCl3
(4)①2Fe2++Br2=2Fe3++2Br- ②2Fe3++ H2SO3= 2Fe2++SO42-+2H+ ③H2SO3>Fe2+>Br-
本题解析:E是红褐色固体,则E是氢氧化铁,氢氧化亚铁和氧气反应生成氢氧化铁,所以D是氢氧化亚铁,B与碱能反应生成氢氧化亚铁,则B是亚铁盐,C是铁盐,,A为单质,则A是铁。
(1)A为Fe,E为Fe(OH)3。
(2)氢氧化亚铁生成氢氧化铁的化学方程式为4Fe(OH) 2+O2+2H2O=4Fe(OH)3。
(3)取少量铁盐溶于水,加入酸化的硝酸银溶液,有白色沉淀生成,说明该物质为氯化铁,则铁生成氯化铁的化学方程式为2Fe+3Cl2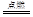 2FeCl3;
2FeCl3;
(4)溶液B是亚铁盐,①滴入溴水时,溶液的颜色变为棕黄色,铁离子棕黄色,说明溴水与亚铁离子反应,离子方程式为2Fe2++Br2=2Fe3++2Br-。②滴入亚硫酸时,溶液由棕黄色变为浅绿色,说明亚硫酸能将Fe3+还原成Fe2+,该反应的离子方程式为2Fe3++ H2SO3= 2Fe2++SO42-+2H+。③根据还原剂的还原性大于还原产物的还原性,由此可知,Fe2+、Br-、H2SO3还原性由强到弱的顺序是H2SO3>Fe2+>Br-.
考点:考查铁及其化合物的化学性质,氧化还原反应等知识。
本题难度:困难
2、填空题 (8分)实验室里迅速制备少量氯气可利用以下反应:
2 KMnO4+16 HCl ="==" 2 KCl + 2 MnCl2 + 5 Cl2↑ + 8 H2O
此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
(1)用“线桥法”表示出电子转移情况:
2 KMnO4+16 HCl ="==" 2 KCl + 2 MnCl2 + 5 Cl2↑ + 8 H2O
(2)该反应中,氧化剂是__________,还原剂是?_________。
(3) 当电子转移的数目为6.02×1023个时生成的氯气的物质的量为 ?mol
参考答案:(8分)
(1) (2分)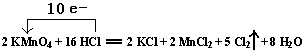 (单、双线桥皆可)?
(单、双线桥皆可)?
(2) (每空2分)? KMnO4?; HCl? (3) (2分)? 0.5
本题解析:(1)“线桥法”表示电子转移情况,可以用“双线桥”也可以用“单线桥”。注意单线桥是直接由还原剂指向氧化剂,标明电子转移数目,不要标得失;
(2)氧化剂是得电子的物质,化合价降低,由方程式知道,Mn元素的化合价降低,则KMnO4是氧化剂,HCl是还原剂。
(3)该反应中16个HCl参与反应,转移10个e-,生成5个Cl2。则转移6.02×1023个电子,即1mol电子时,生成Cl2为0.5mol。
点评:双线桥要会熟练书写,注意检查得失电子总数相等的规律
本题难度:一般
3、填空题 (8分)(1)(NH4)2SO4在强热条件下,可分解生成NH3、SO2、N2、H2O.
反应中氧化产物和还原产物的物质的量之比为?。
(2)将K2S跟HNO3反应,生成NO、S、KNO3、H2O,反应的化学方程式为?;氧化产物是?;?若生成2molNO,反应中电子转移的总物质的量为?mol。
参考答案:(1)1:3(2)3K2S+8HNO3=2NO+3S+6KNO3+4H2O?S? 6
本题解析:略
本题难度:简单
4、选择题 根据以下几个反应:
①Cl2+2KBr=2KCl+Br2 ②Br2+2KI=2KBr+I2 判断氧化性由强到弱的顺序是
[? ? ]
A.I2>Br2>Cl2
B.Cl2>Br2>I2
C.Br2>I2>Cl2
D.Cl2>I2>Br2
参考答案:B
本题解析:
本题难度:一般
5、填空题 亚硫酸根离子(SO32-)具有比SO2更强的还原性,如Na2SO3很容易被空气中的O2氧化为Na2SO4,该反应的化学方程式为:______.实验室为验证Na2SO3常温下容易被氧化,可将Na2SO3溶液加入溴水中,能说明Na2SO3容易被氧化的现象是______,有关离子方程式为:______.
参考答案:①根据题意知,亚硫酸钠有强还原性,溴有强氧化性,所以亚硫酸钠和氧气能发生氧化还原反应,反应物是亚硫酸钠和氧气,产物是硫酸钠,所以该反应的化学方程式为:
2Na2SO3+O2=2Na2SO4
②溴水是橙黄色,亚硫酸钠和溴能发生氧化还原反应,生成硫酸钠和氢溴酸,氢溴酸、硫酸钠的溶液都是无色的,所以看到的现象是溴水褪色;
溴是单质写化学式,水是弱电解质,亚硫酸钠、硫酸钠、氢溴酸是可溶性的强电解质写化学式,所以该离子方程式为:SO32-+Br2+H2O=SO42-+2H++2Br-
故答案为:2Na2SO3+O2=2Na2SO4;溴水褪色;SO32-+Br2+H2O=SO42-+2H++2Br-
本题解析:
本题难度:一般