1��ѡ���� ���з�Ӧ������������ԭ��Ӧ���������������ķ�Ӧ�ǣ�������
A������̫���ܵ���ṩ�ĵ��ܵ��ˮ��������������
B�����������ˮ��ˮ�½��Ϳɴ�0������
C�����������Ľᾧˮ������Ȼ�粒����Ϸ�Ӧ
D������������������������ĩ�������ȷ�Ӧ
�ο��𰸣�A������̫���ܵ���ṩ�ĵ��ܵ��ˮ��������������Ϊ���ȷ�Ӧ��H��OԪ�صĻ��ϼ۷����仯��Ϊ������ԭ��Ӧ����A��ȷ��
B�����������ˮΪ�������̣��Ȳ������ȷ�ӦҲ����������ԭ��Ӧ����B����
C�����������Ľᾧˮ������Ȼ�粒����Ϸ�ӦΪ���ȷ�Ӧ��������������ԭ��Ӧ����C����
D�����ȷ�ӦΪ���ȷ�Ӧ����D����
��ѡA��
���������
�����Ѷȣ���
2������� ʵ�����Ʊ������Ļ�ѧ����ʽΪMnO2+4HCl��Ũ��
MnCl2+Cl2��+2H2O���÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ______���뽫�û�ѧ����ʽ��дΪ���ӷ���ʽ______�������Ĺ�ҵ�Ʒ��ǵ�ⱥ��ʳ��ˮ�����оٳ������������������е�Ӧ�ã�������______������ͨ����ɫʯ����Һ�пɹ۲쵽��������______��
�ο��𰸣��ٸ÷�Ӧ�У�MnO2 ��MnCl2��MnԪ����+4�ۡ�+2�ۣ���2�����ӣ�����MnO2����������
HCl��Ũ����Cl2��ClԪ����-1�ۡ�0�ۣ�ʧ���ӣ����� HCl�ǻ�ԭ����HCl��MnCl2��ClԪ�صĻ��ϼ�û�仯������HCl����μӷ�Ӧ�������������뻹ԭ�������ʵ���֮����1��2��
����������ʡ��������д��ѧʽ�������Ե�ǿ�����д���ӣ�
��������ˮ��Ӧ���ɴ����ᣬ��������ǿ�����ԣ���������������Ӧ���ɴ�����ƣ����������Ư�۵���Ч�ɷ֣�
��������ˮ��Ӧ�ķ���ʽΪ��Cl2+H2O=H++Cl-+HClO��H+��ʹ��ɫʯ���ɺ�ɫ��
HClO? ��ʹ��ɫ������ɫ�����Կ����������ǣ�ɫʯ����Һ�ȱ�����ɫ��
�ʴ�Ϊ��1��2��4H++2Cl-+MnO2?��?.?Mn2++Cl2��+2H2O������ˮ��������Ư�۵ȣ���ɫʯ����Һ�ȱ�����ɫ��
���������
�����Ѷȣ�һ��
3��ѡ���� ���з�Ӧ������������ԭ��Ӧ�����ڷֽⷴӦ���ǣ�������
A��Zn+H2SO4=ZnSO4+H2��
B��2KClO3
2KCl+3O2��
C��S+O2SO2
D��CaCO3CaO+CO2��
�ο��𰸣�A��Zn+H2SO4=ZnSO4+H2�������û���Ӧ��Ҳ����������ԭ��Ӧ����A��ѡ��
B��2KClO3MnO2.��2KCl+3O2�����ڷֽⷴӦ��Ҳ����������ԭ��Ӧ����Bѡ��
C��S+O2?��ȼ?.?SO2���ڻ��Ϸ�Ӧ��Ҳ����������ԭ��Ӧ����C��ѡ��
D��CaCO3?����?.?CaO+CO2�����ڷֽⷴӦ����û��Ԫ�صĻ��ϼ۱仯������������ԭ��Ӧ����D��ѡ��
��ѡB��
���������
�����Ѷȣ���
4������� �����������Ԫ�أ��纬�������Ӱ�������֬��Ĵ�л����������������ж����йغ�����������ת����ϵ����
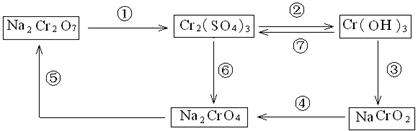
�ش��������⣺
��1������ת����ϵ������������ԭ��Ӧ����______�����ţ���
��2����Ӧ���ǿ��淴Ӧ�����ɫ��Na2CrO4��Һ�м���ϡ���ᣬ��Һ��ɳ�ɫ��д���÷�Ӧ�����ӷ���ʽ______��
��3����ͼʾ��Ϣ��֪����һ�ֺ��������������ԣ�д���û�������NaOH��Һ��Ӧ�����ӷ���ʽ��______��
��4����֪Ag2CrO4��AgCl��Ksp�ֱ�Ϊ9.0��10-12��1.56��10-10��������ͬŨ�ȵ�Na2CrO4��NaCl�Ļ����Һ����μ�����������Һ���������ɵij�����______��
��5����ҵ�ϴ�����Cr2O72-�ķ�ˮʱ��һ�㽫�綾��Cr2O72-ת��ΪCr3+����ԭ������̼��������������������⺬NaCl��Cr2O72-�����Է�ˮ��
д���缫��Ӧ����Һ�н��еķ�Ӧ�����ӷ���ʽ��
����______������______����Һ��______��
�ο��𰸣���1�����ͼ�е�ת����ϵ����Ԫ�ػ��ϼ۱仯�ķ�Ӧ�Ǣ٢ܢޣ�������������ԭ��Ӧ���ʴ�Ϊ���٢ܢޣ�
��2������ͼ�е�ת����ϵ�ݣ���֪����������Ի����¿��Ա���ظ��������ɫ��Һ��ɳ�ɫ��ʵ���ǣ�2CrO42-+2H+
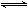
?Cr2O72-+H2O���ʴ�Ϊ��2CrO42-+2H+
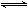
?Cr2O72-+H2O��
��3������ͼʾת����ϵ�ۢߣ�����֪��Cr��OH��3���ܺ�ǿ�ᷴӦ���ܺ�ǿ�Ӧ����ǿ�Ӧ��ʵ���ǣ�Cr��OH��3+OH-=CrO2-+2H2O���ʴ�Ϊ��Cr��OH��3+OH-=CrO2-+2H2O��
��4��Ag2CrO4��AgCl��Ksp�ֱ�Ϊ9.0��10-12��1.56��10-10��������ͬŨ�ȵ�Na2CrO4��NaCl�Ļ����Һ����μ�����������Һ��
��Na2CrO4��NaCl��Ũ�ȶ�Ϊ1mol/L��Ag2CrO4����ʱ��Ҫ��c��Ag+��=
���������
�����Ѷȣ�һ��
5������� �������������ʣ�NO��Cu��NO3��2��Cu2O��HNO3�Ļ�ѧʽ�ֱ����ڿհ״��������һ����ƽ�˵Ļ�ѧ����ʽ������֪�����ԣ�HNO3��Cu��NO3��2��______+______��______+______+H2O
��1���÷�Ӧ�еĻ�ԭ����______��
��2���÷�Ӧ�У�������ԭ��Ӧ��Ԫ����______��
�ο��𰸣�NO��NԪ�ػ��ϼ�Ϊ+2��HNO3��NԪ�ػ��ϼ�Ϊ+5��Cu��NO3��2��CuԪ�ػ��ϼ�Ϊ+2��Cu2O��CuԪ�ػ��ϼ�Ϊ+1����
�����ԣ�HNO3��Cu��NO3��2�������������������õ�������NO����Cu2Oʧ���ӻ��ϼ���������ԭ��������Cu��NO3��2��
���Ը÷�Ӧ����ʽΪ��3Cu2O+14HNO3�T6Cu��NO3��2+2NO��+7H2O��
�ʴ�Ϊ��3Cu2O��14HNO3��6Cu��NO3��2��2NO����
��1���÷�Ӧ��������ͭʧ���ӻ��ϼ����ߣ�����������ͭ����ԭ�����ʴ�Ϊ��Cu2O�� ?
��2���÷�Ӧ��������NԪ�صõ��ӻ��ϼ۽��ͣ�����NԪ�ط�����ԭ��Ӧ���ʴ�Ϊ��N��
���������
�����Ѷȣ�һ��