1、选择题 下列说法正确的是 (? )
A.从海水中提取物质都必须通过化学反应才能实现
B.二氧化硫可用于消毒杀菌和漂白纸张草帽等
C.过氧化钠、烧碱、纯碱分别属于碱性氧化物、碱、盐
D.Na、Al、Cu可以分别用热还原法、热分解法和电解冶炼法得到
参考答案:B
本题解析:从海水中提取蒸馏水和盐时,通过蒸馏、蒸发等物理变化就能实现,提取溴、碘、镁等物质时,必须通过化学反应才能实现,A项错误;二氧化硫具有还原性,能够使一些物质褪色,因而具有漂白性且可用于消毒杀菌,B项正确;过氧化钠属于过氧化物,C项不正确;金属冶炼方法常用的有三种:①热分解法,适用于制取不活泼金属如Ag等;②热还原法,适用于制取金属活动性顺序表中Al以后、Hg以前的金属;③电解法,适用于制取金属活动性顺序表中Al及以前的还原性很强的金属,D项错误。
本题难度:一般
2、选择题 已知A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,原子半径按D、E、B、C、A的顺序依次减小,B、E同主族,下列推断正确的是
[? ]
A.? A、B、E一定不在同一周期
B.? D为第二周期元素
C.? A、D不可能在同一主族
D.? C、D的单质化合一定形成离子化合物
参考答案:A
本题解析:
本题难度:一般
3、选择题 下列物质性质递变正确的是
[? ]
A.原子半径:C、Al、K依次增大
B.热稳定性:HF、NH3、SiH4依次增强
C.水化物的酸碱性:NaOH、Al(OH)3、Mg(OH)2碱性减弱
D.非金属性:Cl、P、S依次增强
参考答案:A
本题解析:
本题难度:一般
4、推断题 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的原子序数依次增大。其中A、C原子的L层有2个未成对电子。D与E同主族,D的二价阳离子与C的阴离子具有相同的电子层结构。F3+离子M层3d轨道电子为半满状态。请根据以上情况,回答下列问题(答题时,用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为_________________。
(2)A的氢化物的分子空间构型是________,其中心原子采取__________杂化,属于__________(填“极性分子”和“非极性分子”)。
(3)F和M(质子数为25)两元素的部分电离能数据列于下
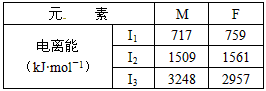
|
比较两元素的I2、I3可知,气态M2+再失去一个电子比气态F2+再失去一个电子难。对此,你的解释是
______________________;
(4)晶体熔点:DC________EC(填“<、=、>”),原因是_______________________。
(5)H2S和C元素的氢化物(分子式为H2C2)的主要物理性质比较如下

H2S和H2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因__________________________
(6)已知某化合反应,在反应过程中只有σ键的断裂与生成,写出符合要求的化学方程式 (写一个)
__________________________
参考答案:(1)C<O<N
(2)正四面体;sp3杂化;非极性分子
(3)Mn2+的3d轨道电子排布为半满状态较稳定
(4)>;MgO与CaO都为离子晶体,Mg2+半径小于Ca2+,则MgO的晶格能大于CaO,所以熔点高
(5)H2O2分子间存在氢键,与水分子可形成氢键
(6)“略”
本题解析:
本题难度:困难
5、选择题 下列各组单质中,前者能将后者从化合物中置换出来的是
①Al、Fe? ②H2、Cu? ③Mg、C? ④C、Na
A.只有①②?B.只有②③?C.只有①②③?D.①②③④
参考答案:C
本题解析:金属铝的活泼性强于铁,因此铝单质可以从铁的氧化物中置换出单质铁,①正确;氢气具有还原性,能把氧化铜中铜置换出来,②正确;镁是活泼的金属,能和CO2反应生成氧化镁和单质碳,③正确;碳是非金属性,钠是活泼的金属,碳不可能从钠的化合物中置换出金属钠,金属钠的冶炼只能通过电解法,④不正确,答案选C。
本题难度:一般