| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ�㽲�⡶ԭ���ԭ����������ѵ��2019�����°棩(��)
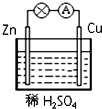 �ο��𰸣�ͼΪͭпԭ��أ�Zn��Cu���ã�ӦΪԭ��صĸ�����������ӦΪZn-2e-�TZn2+�� ��������� �����Ѷȣ�һ�� 3��ѡ���� ��ҵ������������������ȼ�գ����ò���������ˮ�ķ����Ƶù�ҵ�����ᣬ���̸�������������˷ѡ�������������ԭ���ԭ��ֱ���������ͬʱ����ȡ���ܣ����������뷨���У�����˵���϶�������� �ο��𰸣�B ��������� �����Ѷȣ�һ�� 4������� ij����С������ͼ����ʵ�飬�Իش��������⣮ �ο��𰸣���1������ʼʱ����K��a���ӣ���װ�ù���ԭ��أ�����ʧ���Ӷ���������ʯī����������������ʧ���ӷ���������Ӧ���缫��ӦʽΪFe-2e-=Fe2+�� ��������� �����Ѷȣ��� 5������� �����Ͻ����κ��Է���������ԭ��Ӧ��������Ƴ�ԭ��ء������÷�Ӧ��Cu��2Ag+ ��2 Ag +Cu2+ ������һ����ѧ��أ�����������̼�������ش��������⣺ �ο��𰸣�(1)������ ��������Ӧ�� Cu -2e-��Cu2+ ���������ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ���ݴ˿�֪ͭ�Ǹ�����ʧȥ���ӣ�����������Ӧ���缫��Ӧʽ��Cu -2e-��Cu2+���������������õ����ӣ���˵������ҺӦ������������Һ�� �����Ѷȣ�һ�� |
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ���ȫ��������Ⱦ��.. | |
| �����Ŀ |