1、填空题 (1)共价键的____和____反映了共价键的强弱程度,________和________常被用来描述分子的空间构型。
(2)sp杂化轨道是由一个____和一个____组合而成的。每个sp杂化轨道含有1/2s和1/2p的成分。sp杂化轨道间的夹角为________,呈________型,如________。
(3)sp3杂化轨道是由一个____和________组合而成,每个sp3杂化轨道含1/4s和3/4p的成分,sp3杂化轨道间的夹角为_______,呈_______型,如________。
参考答案:(1)键长;键能;键长;键角
(2)s轨道;p轨道;180°;直线;CO2、BeCl2、C2H2
(3)s轨道;3个p轨道;109.5°;四面体;CH4、CCl4
本题解析:
本题难度:一般
2、选择题 有关甲醛分子(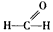 )的说法正确的是
)的说法正确的是
[? ]
A.C原子采取sp杂化
B.甲醛分子为三角锥形结构
C.C原子采取sp2杂化
D.甲醛分子为平面三角形结构
参考答案:CD
本题解析:
本题难度:简单
3、选择题 下列分子的中心原子发生sp2杂化的是( )
A.CH4
B.NH3
C.H2O
D.BF3
参考答案:D
本题解析:
本题难度:简单
4、简答题 下列是A、B、C、D、E五种短周期元素的某些性质
| A | B | C | D | E
化合价
-4
-2
-1
-2
-1
电负性
2.5
2.5
3.0
3.5
4.0
|
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是______
A.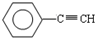 B.CH4C.CH2=CHCH3 D.CH3CH2C≡CHE.CH3CH3
B.CH4C.CH2=CHCH3 D.CH3CH2C≡CHE.CH3CH3
(2)与AD2互为等电子体的分子、离子的化学式依次为______、______(各写1种)
(3)相同条件下,AD2与BD2分子两者在水中的溶解度较大的是______(写分子式),理由是______.
参考答案:A、B、C、D、E五种短周期元素,根据元素化合价知,A属于第ⅣA族,B、D属于第ⅥA族,C、E属于第VⅡA族,B的电负性小于D,所以D是O元素,B是S元素;C的电负性小于E,所以C是Cl元素,E是F元素,硅的电负性小于S,A的电负性等于S元素,所以A是C元素,
(1)A.苯环上碳原子含有3个σ 键,采用sp2杂化,故A错误;
B.甲烷分子中碳原子含有4个σ 键,采用sp3杂化,故B错误;
C.丙烯中甲基碳原子含有4个σ 键,采用sp3杂化,碳碳双键两侧的碳原子含有3个σ 键,采用sp2杂化,故C错误;
D.1-丁炔中甲基和亚甲基中碳原子含有4个σ 键,采用sp3杂化,碳碳三键两侧的碳原子含有2个σ 键,采用sp杂化,故D正确;
E.乙烷中甲基碳原子含有4个σ 键,采用sp3杂化,故E错误;
故选D;
(2)与CO2互为等电子体的分子、离子中含有3个原子,16个价电子,所以其等电子体的分子、离子的化学式依次为N2O、SCN-,故答案为:N2O、SCN-;
(3)相同条件下,CO2与SO2分子两者在水中的溶解度较大二氧化硫,二氧化碳是非极性分子,二氧化硫是极性分子,水是极性分子,根据“相似相溶”原理知,SO2在H2O中的溶解度较大,
故答案为:SO2,因为CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”原理,SO2在H2O中的溶解度较大.
本题解析:
本题难度:简单
5、填空题 硼的单质和化合物在工业上有重要的应用。
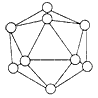
(1)晶体硼的基本结构单元都是由硼原子组成的正二十面体,其中含有20个等边三角形的面和一定数目的顶角,每个顶角各有一个硼原子。如图所示,则针对晶体硼的基本结构单元回答下列问题:
①B-B键间键角为_________;
②其中硼原子数有________个;B-B键有________根。
(2)B2O3与C3O2互为等电子体,试写出C3O2的结构式___________。
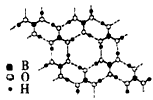
(3)硼酸[B(OH)3]是一种较弱的一元酸,眼科医院常用作消毒剂,在实验中不小心被碱溶液灼伤后清洗伤口后可涂上少量的硼酸,写出硼酸的电离方程式____________。在硼酸分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是
_______。
A.sp,范德华力 B.sp2,范德华力 C.sp2,氢键 D.sp3,氢键
(4)在30℃以下,将过氧化氢加到硼酸和氢氧化钠的混合溶液中,析出一种无色晶体X。组成分析证实,该晶体的质量组成为Na 14. 72%,B 7.03%, H 5.12 %,则X的化学式为________。
参考答案:(1)①60°;②12;30
(2)O=C=C=C=O
(3)B(OH)3+H2O [B(OH)4]-+H+;C
[B(OH)4]-+H+;C
(4)NaBH8O7或NaBH2O4・3H2O
本题解析:
本题难度:一般