1������� ��ͼ��һ���Ҵ�ȼ�ϵ�ع���ʱ��ʾ��ͼ���ҳ��е������缫һ����ʯī�缫��һ�������缫������ʱM��N�����缫�������������٣���ش��������⣺
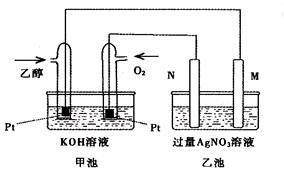
��1��M�缫�IJ�����??���缫������?��N�ĵ缫��ӦʽΪ?�������Ҵ��IJ��缫�ĵ缫��Ӧʽ?��
��2���ڴ˹����У��ҳ���ijһ�缫����������4.32gʱ���׳�����������������Ϊ??L����״���£�������ʱ�ҳ���Һ�����Ϊ400mL�����ҳ�����Һ��pHΪ?��
��3�����ڳ��³�ѹ�£�1g C2H5OHȼ������CO2��Һ̬H2Oʱ�ų�29.71kJ��������ʾ�÷�Ӧ���Ȼ�ѧ����ʽΪ??��
�ο��𰸣���1����?����? 4OH����4e��? 2H2O+O2��
C2H5OH��12e+16OH��=2CO32��+11H2O��2�֣�
��2��0.224 ?1
��3��C2H5OH��l��+3O2��g��? 2CO2��g��+3H2O��l����H=��1366.7kJ/mol
�����������
�����Ѷȣ�һ��
2��ѡ���� ������пƬ��ͭƬ��ϡ������ɵ�ԭ��ص�˵���У���ȷ����
A��пƬ�������٣�ͭƬ�������ݲ���
B��������������пƬ����ͭƬ
C��пƬ��������������ԭ��Ӧ
D���������Һ��pH���ֲ���
�ο��𰸣�A
�����������ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ������������ƶ��������õ����ӣ�������ԭ��Ӧ��п��ͭ���ã�п�Ǹ�����ͭ����������Һ�е��������������ŵ硣����ѡ��A��ȷ��
�����Ѷȣ�һ��
3������� ��4�֣���1����֪��һ����CH4��ȫȼ������CO2��Һ̬ˮʱ���ų�����QkJ������ȼ�ղ���ȫ��ͨ������ij���ʯ��ˮ���ɵõ�20g��������д��CH4ȼ�յ��Ȼ�ѧ����ʽ?
?
��2����д��������ȼ�ϵ�ص������缫��Ӧʽ���������ҺΪϡ���ᣩ?
�ο��𰸣���1��CH4(g)+2O2(g)=CO2(g)+2H2O(l)? ��H= -5QkJ/mol?��2�֣�
��2��O2+4H++4e-=2H2O?��2�֣�
�����������1��20g������̼��ƣ����ʵ�����0.2mol�����Ը���̼ԭ���غ��֪ȼ�����ɵ�CO2Ҳ��0.2mol����������1molCO2�ų���������5QkJ������Ȼ�ѧ����ʽΪ
CH4(g)+2O2(g)=CO2(g)+2H2O(l)? ��H= -5QkJ/mol��
��2��ԭ��������ǵõ����ӵģ�����������ȼ�ϵ��������������ͨ�룬������Һ�����ԣ����������缫��ӦʽΪO2+4H++4e-=2H2O��
�����Ѷȣ�һ��
4������� �ס������ص缫������ͼ��ʾ���밴Ҫ��ش��������⣺
��1���������о�ΪCu��NO3��2��Һ����Ӧһ��ʱ���
���к�ɫ�����������Ǽ׳��е�______��������̼�����ҳ��е�______��������������
���ҳ��������Ϸ����ĵ缫��Ӧ����ʽ��______��
��2���������о�Ϊ����NaCl��Һ��
��д���ҳ����ܷ�Ӧ�Ļ�ѧ����ʽ______��
�ڼ׳���̼���ϵ缫��Ӧ����ʽ��______���ҳ�̼���ϵ缫��Ӧ����______����������Ӧ����ԭ��Ӧ����
�ο��𰸣���û����ӵ�Դ��������ԭ��أ�����������̼��������������ӵ�Դ�������ǵ��أ����ݵ��ӵ������жϣ�����������̼��������
��1���ټ׳��е�?����������ԭ��Ӧ���н���������������̼����
�ҳ��е�����������ԭ��Ӧ���н���������������������
�ʴ�Ϊ��̼������
���ҳ��������Ϸ���������Ӧ�����������ӵķŵ�����������������ӵķŵ�����������������������ʧ��������������ˮ���ʴ�Ϊ��4OH--4e-�TO2��+2H2O
��2�����Ȼ�����Һ�д��ڵ������ǣ������ӡ����������ӡ������ӡ������ӣ������ӵķŵ������������������ӣ������ӵķŵ��������������ӣ����Ը÷�Ӧ�����������������������������ƣ�
�ʴ�Ϊ��2H2O+2NaCl??���?.?2NaOH+H2��+Cl2��
����������Һ�У�����һ��������������ʱ�ᷢ��������ʴ����������ʧ���ӣ�������������ˮ�õ����������������ӣ��ҳ���̼���������������Ϸ���������Ӧ��
�ʴ�Ϊ��O2+4e-+2H2O�T4OH-��������Ӧ��
���������
�����Ѷȣ�һ��
5��ѡ���� ���и�װ���о�ʢ��ϡ���ᣬ���в��ܹ���ԭ��ص���
[? ]
A��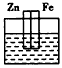
B��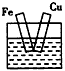
C��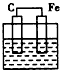
D��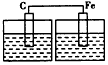
�ο��𰸣�D
���������
�����Ѷȣ���