1、选择题 如图为原电池示意图,下列说法中正确的是
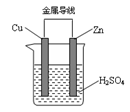
A.锌片是正极
B.铜片上发生的反应为:Cu-2e- ="=" Cu2+[来
C.电子由锌片通过导线流向铜片
D.该装置能够将电能转化为化学能
参考答案:C
本题解析:A.不正确,锌片是负极; B.不正确,铜片上发生的反应为:2H++2e- ==H2↑
C.正确;D.不正确,该装置能够将化学能转化为电能;选C。
本题难度:一般
2、选择题 下列叙述正确的是
A.碱性锌锰干电池的负极材料为二氧化锰
B.碱性氢氧燃料电池工作时负极反应为:H2-2e-+2OH-=2H2O
C.铅蓄电池放电时负极反应为:PbO2+2e-+4H+=Pb2+++2H2O
D.锌一铜一稀硫酸构成的原电池工作时,H+向负极移动
参考答案:B
本题解析:略
本题难度:一般
3、选择题 某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( )
A.正极反应式为:O2+2H2O+4e-=4OH-
B.工作一段时间后,电解液中KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2=2H2O
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
参考答案:D
本题解析:把释放能量的氧化还原反应:2H2+O2=2H2O通过电池反应进行就制得氢氧燃料电池。H2失去电子,在负极上被氧化,产生H+,由于电解液中有大量的OH-,所以电极反应式为:2H2-4e-+4OH-=4H2O。工作一段时间后,KOH溶液被稀释,但KOH的物质的量不变。D项,n(Cl2)=0.1 mol,转移电子0.2 mol。
本题难度:一般
4、填空题 铁单质及其化合物在生活、生产中应用广泛。请回答下列问题:
(1)钢铁在空气中发生吸氧腐蚀时,正极的电极反应式为__________________。
(2)由于氧化性Fe3+>Cu2+,氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是________________________________。
(3)硫酸铁可作絮凝剂,常用于净水,其原理是_______________________(用离子方程式表示)。在使用时发现硫酸铁不能使酸性废水中的悬浮物沉降而除去,其原因是________________________________________。
(4)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO===3Fe+4CO2,若有
1.5?mol?Fe3O4参加反应,转移电子的物质的量是__________________。
参考答案:(1)O2+2H2O+4e-===4OH-
(2)2Fe3++Cu===2Fe2++Cu2+?
(3)Fe3++3H2O Fe(OH)3(胶体)+3H+;酸性环境中,H+抑制了铁离子的水解,无法生成氢氧化铁胶体
Fe(OH)3(胶体)+3H+;酸性环境中,H+抑制了铁离子的水解,无法生成氢氧化铁胶体
(4)12?moL
本题解析:
本题难度:一般
5、填空题 如下图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题。
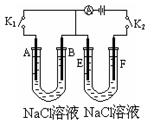
(1)打开K2,合并K1。B为?极,A的电极反应为?,最终可观察到的现象是?
涉及的化学反应方程式有:?
(2)打开K1,合并K2。E为?极,F极的电极反应?为?,检验F极产生气体的方法是?。
(3)若往U型管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是?,原因是?
参考答案:

本题解析:略
本题难度:一般