1、选择题 下列说法错误的是
A.在C(s) +H2O(g) 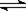 CO(g) + H2(g)反应体系中,增加碳的量不能迅速提高正反应速率
CO(g) + H2(g)反应体系中,增加碳的量不能迅速提高正反应速率
B.钾的金属性比钠强,所以钾与水的反应比钠的反应剧烈
C.在压强相同条件下,结构相似的CH4、SiH4、GeH4的沸点依次升高,所以结构相似的HF、HCl、HBr、HI的沸点也依次升高
D.面粉厂严禁烟火的原因是面粉粉尘表面积大,与空气接触遇明火极易发生爆炸
参考答案:C
本题解析:略
本题难度:简单
2、选择题 一定量的稀盐酸跟过量锌粉反应时,为了减缓反应速率又不影响生成H2的总量,可采取的措施是( )
A.加入少量醋酸钾固体
B.加入少量稀NaOH溶液
C.加入少量NH4HSO4固体
D.加入少量Na2CO3浓溶液
参考答案:A.加入少量CH3COOK固体,使盐酸转化为醋酸,减小氢离子的浓度,不改变氢离子的物质的量,可满足减缓反应速率但又不影响生成H2的总量,故A选;
B.因盐酸与NaOH溶液反应,会导致生成氢气的量减少,故B不选;
C.因为硫酸氢钠溶液中含有氢离子,会导致生成氢气的量增多,故C不选;
D.因为盐酸和碳酸钠溶液反应,会导致生成氢气的量减少,故D不选;
故选A.
本题解析:
本题难度:一般
3、选择题 在2A+B=3C+4D的反应中,下列表示该反应速率最大的是( )
A.V(C)=0.5mol/(L?min)
B.V(A)=0.8mol/(L?min)
C.V(B)=0.3mol/(L?min)
D.V(D)=1mol/(L?min)
参考答案:对于反应2A+B=3C+4D,都转化为D表示的速率进行比较,
A.V(C)=0.5mol/(L?min),反应速率之比等于其计量数之比,故V(D)=43V(C)=0.67mol/(L?min);
B.V(A)=0.8mol/(L?min),反应速率之比等于其计量数之比,故V(D)=2V(A)=1.6mol/(L?min);
C.V(B)=0.3mol/(L?min),反应速率之比等于其计量数之比,故V(D)=4V(A)=1.2mol/(L?min);
D.V(D)=1mol/(L?min),
故选:B.
本题解析:
本题难度:简单
4、选择题 在2CH4(g)+2NH3(g)+3O2(g)=2HCN(g)+6H2O(g)反应中,已知v(HCN)=nmol/(L?min),且v(O2)=mmol/(L?min),则m与n的关系正确的是( )
A.m=
n
B.m=n
C.m=n
D.m=2n
参考答案:已知:v(HCN)=nmol/(L?min),v(O2)=mmol/(L?min),
反应速率之比等于其计量数之比,故nmol/(L?min):mmol/(L?min)=2:3,即m=32n,
故选:C.
本题解析:
本题难度:一般
5、选择题 下列说法正确的是
A.常温下,中和pH与体积均相同的盐酸和醋酸消耗NaOH的物质的量相同
B.纯铁和生铁在酸雨中均发生电化学腐蚀
C.使用催化剂不但能加快反应速率,而且可以让不可能发生的反应发生
D.食品工业用NaHCO3作焙制糕点的膨松剂
参考答案:D
本题解析:A、醋酸是弱酸,部分电离,pH相同的盐酸与醋酸中是醋酸浓度远大于盐酸,体积相同时消耗NaOH是醋酸远大于盐酸,错误;B、纯铁只含铁不能构成原电池,发生化学腐蚀,生铁中碳与铁构成原电池,发生电化学腐蚀,错误;C、催化剂只能降低活化能,从而改变反应速率,不能改变反应热能,更不能使不能发生的反应发生,错误;D、NaHCO3受热或能与酸反应产生CO2,能使食物蓬松,正确。3的用途。
本题难度:一般