| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《化学反应速率》典型例题(十)
参考答案:D 本题解析:化学反应速率之比等于化学计量数之比,所以3v正(NH3)=2v正(H2O),A项错误;生成NO表示V (正),而消耗NH3指的是V (正),B项错误;增大容器的体积,正反应速率增大,逆反应速率也增大, C项错误;达到化学平衡时4v正(O2)=5v逆(NO),说明反应达到化学平衡状态,D项正确;选D。 本题难度:一般 4、选择题 反应2SO2+O2?2SO3经一段时间后,SO3的浓度增加了0.4mol?L-1,在这段时间内用O2表示的反应速率为0.04mol?L-1?s-1,则这段时间为( ) 参考答案:用O2表示的反应速率为0.04mol?L-1?s-1, 本题解析: 本题难度:一般 5、实验题 H2O2是实验室常用的一种化学试剂。某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。分析下图能够得出的结论是 。 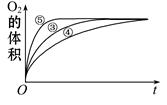 (3)为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如下图所示的实验装置进行实验。 实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,则实验中需要测量的数是 。 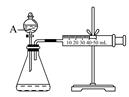 (4)H2O2能氧化H2SO4 酸化的FeSO4,离子方程式为 ; 参考答案:(8分)(1)探究H2O2溶液的浓度的变化对分解速率的影响。 本题解析:(1)根据表中数据可知,实验①②中不同之处在于双氧水的浓度不同,所以实验目的是探究H2O2溶液的浓度的变化对分解速率的影响。 本题难度:困难 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《原电池原理》试题.. | |