1、选择题 下列物质中属于电解质的是( )
①氢氧化钠?②硫酸钡?③铜?④蔗糖?⑤二氧化硫?⑥盐酸.
A.①②
B.①②⑥
C.③④
D.①⑤
参考答案:A
本题解析:
本题难度:简单
2、选择题 下列各项中的物质能导电且属于强电解质的是
A.固态氯化镁(MgCl2)
B.液态氯化镁(MgCl2)
C.氨水
D.液态H3PO4
参考答案:B
本题解析:本题主要考查电解质、强电解质、弱电解质等概念以及电解质导电的条件.MgCl2是强电解质,但固态的MgCl2不导电,液态的MgCl2能导电.氨水能导电,但氨水中的主要成分是H2O和NH3・H2O,故氨水为混合物,不能将氨水叫电解质.H3PO4是弱电解质,但纯的液态H3PO4不导电,只有在水溶液里才能导电.
本题难度:困难
3、选择题 想一想:氢氧化钡(液态)、硫酸铜(固态)、纯醋酸这些物质为什么归为一类,下列哪种物质还可以和它们归为一类
[? ]
A.C2H5OH(液态)
B.HCl(气态)
C.氯化钠溶液
D.豆浆
参考答案:B
本题解析:
本题难度:简单
4、填空题 常温下,在20.0 mL 0.20 mol/L CH3COONa溶液中滴加0.20 mol/L的稀盐酸。溶液的pH的变化关系如下图所示。
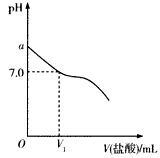
(1)a>7.0的理由是__________________(用离子方程式表示)。
(2)如图,当加入稀盐酸的体积为V1mL时,溶液的pH刚好为7.0。此时溶液中c(Cl-)___c(CH3COOH)(填 “<”、“>”或“=”)。简要写出判断依据:_____________________。
(3)当加入盐酸的体积为20.0 mL时,测得溶液中的c(H+)为1.3×10-3 mol/L,则CH3COOH的电离平衡常数Ka=_______(计算结果保留两位有效数字)。
参考答案:(1)CH3COO-+H2O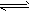 CH3COOH+OH-;
CH3COOH+OH-;
(2)=;根据电荷守恒有:c(OH-)+c(Cl-)+c(CH3COO-)=c(H+)+c(Na+),由于溶液的pH=7,c(OH-)=c(H+),所以c(Cl-) +c(CH3COO-)=c(Na+);而根据物料守恒有:c(CH3COOH)+c(CH3COO-)=c(Na+),所以有c(CH3COOH)=c(Cl- )
(3)1.7×10-5
本题解析:
本题难度:一般
5、选择题 下列物质中,能够导电的电解质是
[? ]
A.熔融的MgCl2
B.Cu丝
C.NaCl溶液
D.蔗糖
参考答案:A
本题解析:
本题难度:简单