1、计算题 现有镁、铝的混合物7.8g,与500ml 2mol/L硫酸溶液反应共放出H28.96L(标准状况),求:
(1)混合物中镁的物质的量是多少?
(2)混合物中Al的质量是多少?
(3)反应结束后溶液中氢离子的物质的量浓度是多少?
参考答案:(1)0.1mol
(2)5.4g
(3)2.4mol/L
本题解析:
本题难度:一般
2、选择题 设NA为阿伏加德罗常数的数值,下列说法正确的是 ( )
A.标准状况下,22.4 L CCl4含有4NA个共价键
B.1mol D2O所含的电子总数为12NA
C.常温下,23 g NO2含有NA个氧原子
D.1mol Fe2+与足量的H2O2溶液反应,转移2NA个电子
参考答案:C
本题解析:A.22.4L/mol是在标准状况(0 ℃,1.01×105Pa)下的气体摩尔体积。
B.1mol D2O所含的电子总数为10NA,对于原子,核外电子数=质子数,质子数=核电荷数=原子序数;
D.1mol Fe2+与足量的H2O2溶液反应,生成1mol Fe3+,转移NA个电子。
本题难度:一般
3、计算题 过氧化钙(CaO2)是 一种安全无毒物质,带有结晶水,通常还含有CaO。
(1)称取0.542 g过氧化钙样品,灼热时发生如下反应:2[CaO2・xH2O]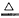 2CaO+O2↑+2xH2O,得到O2在标准状况下的体积为67.2 mL,该样品中CaO2的物质的量为_____________ 。
2CaO+O2↑+2xH2O,得到O2在标准状况下的体积为67.2 mL,该样品中CaO2的物质的量为_____________ 。
(2)另取同一样品0.542 g,溶于适量稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 0.70 g。
①试计算样品中CaO的质量。
②试计算样品中CaO2・xH2O的2x值。
参考答案:(1)0.006 mol
(2)①0.056 g②x=1/2
本题解析:
本题难度:一般
4、实验题 (6分)今有一混合物的水溶液,只可能含有以下离子中的若干 种:Na+、NH4+、Cl-、Cu2+、Fe3+、CO32―、SO42―,现每次取100.00ml进行下列实验:
种:Na+、NH4+、Cl-、Cu2+、Fe3+、CO32―、SO42―,现每次取100.00ml进行下列实验:
①第一份加入AgNO3溶液有沉淀产生.
②第二份加足量NaOH后加热,收集到气体0.896L(标准状态下).
③第三份加足量BaCl2后,得干燥沉淀6.27g,沉淀经足量盐酸洗涤干燥后,剩余2.33g.在原溶液中一定存在的离子及其物质的量浓度分别为:? _______________?.
参考答案:c(NH4+)=0.4mol・L-1,? c(SO?42-)=0.1mol・L-1,? c(CO32-)=0.2mol・L-1,c(Na+)≥0.2mol・L-1?(答错或答不全均不给分)
本题解析:略
本题难度:简单
5、选择题 下列各组物质中,含原子数最多的是( )
A.0.4 mol NH3
B.4 ℃时5.4 mL水
C.10 g氖气
D.6.02×1023个H2SO4分子