1、选择题 下列两种气体的分子数一定相等的是
A.质量相等、密度不等的O2和C2H4
B.等体积等密度的CO和C2H4
C.等温等体积的O2和N2
D.等压等体积的N2和CO2
参考答案:B
本题解析:只要气体分子的物质的量相等,其分子数就一定是相等的。氧气和乙烯的相对分子质量不同,在质量相等的条件下,气体的物质的量不相等,分子数不同;等体积等密度,则质量相等。由于CO和乙烯的相对分子质量都是28,所以选项B中气体的物质的量是相等的,分子数相等;选项C中,压强不一定相同,而选项D中温度不一定相同,所以分子数不一定相同,因此正确的答案选B。
本题难度:一般
2、计算题 (6分)(1)科学研究表明,由于大量使用氟利昂使南极上空的臭氧层出现空洞。臭氧的化学式为O3。在同温同压下,相同质量的O2和O3的物质的量比为 ,
(2)HCl气体极易溶于水,若向水中通入标准状况下的44.8LHCl气体配成1L盐酸,所得盐酸的物质的量浓度为 ;取此盐酸250mL与小苏打(NaHCO3)反应,请计算最多可以产生二氧化碳的体积 (标准状况)。
参考答案:(1)3:2 (2)2.0mol/L 11.2 L
本题解析:(1)根据n=m/M可知,相同质量的物质,其物质的量之比与摩尔质量成反比,故相同质量的O2和O3的物质的量比为48g/mol:32g/mol=3:2;(2)n(HCl)=44.8L÷22.4L/mol=2mol,c=2mol÷1L=2mol/L,设生成的CO2物质的量为n mol
HCl+NaHCO3=NaCl+CO2↑+H2O
1 1
2mol/L×0.25L n 得n ="0.5" mol, V(CO2)=n×22.4L/mol=11.2L。
考点:考查物质的量及在化学方程式中的应用。
本题难度:一般
3、选择题 2.设NA为阿伏加德罗常数,下列说法中正确的是(?)
A.1NA个氢气分子所占的体积为22.4L
B.2NA个二氧化碳分子的质量为44g
C.1000mL0.1mol/L 的NaCl溶液中,Na+与Cl-离子总数为0.2NA
D.17g氨气中所含原子数为NA
参考答案:C
本题解析:略
本题难度:简单
4、选择题 用NA表示阿伏加德罗常数的值。下列叙述正确的是 (? )
(? )
A.标准状况下,5.6L四氯化碳含有的分子数为0.25NA



B.2.8g [CH2 CH2 ]n 中含有的碳原子数为0.2NA
C.分子数为NA的CO、C2H4混合气体体积约为22.4L
D.乙烷和丙烯的物质的量共1mol,完全燃烧生成水分子数为3NA
参考答案:
本题解析:略
本题难度:简单
5、选择题 设NA为阿伏加德罗常数的数值,下列说法正确的是(?)。
A.1 mol・L-1 NaCl溶液含有NA个Na+
B.1 mol Cu和足量稀硝酸反应产生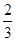 NA个NO分子
NA个NO分子
C.1 L 0.1 mol・L-1氨水含有0.1NA个OH-
D.1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子
参考答案:B
本题解析:由于没有提供1 mol・L-1 NaCl溶液的体积,则溶液所含Na+数目无法确定,A项错误;根据Cu与稀硝酸的反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,则反应生成的n(NO)=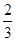 n(Cu),其分子数目为
n(Cu),其分子数目为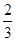 NA,B项正确;C项氨水中的NH3・H2O为弱电解质,不能完全电离,1 L 0.1 mol・L-1氨水中OH-数目小于0.1NA;D项中Fe2+被氧化成Fe3+,1 mol Fe2+转移1 mol电子,即NA个电子。
NA,B项正确;C项氨水中的NH3・H2O为弱电解质,不能完全电离,1 L 0.1 mol・L-1氨水中OH-数目小于0.1NA;D项中Fe2+被氧化成Fe3+,1 mol Fe2+转移1 mol电子,即NA个电子。
本题难度:一般