1、选择题 NO因污染空气而“臭名昭著”,而奇妙的作用也使其成为“明星分子”。如可用于制HNO3、肥料、炸药、促进血管扩张、促进免疫功能、增强记忆等。下列各组物质中,不能生成NO的是(?)
A.Cu + HNO3(稀)
B.N2 + O2
C.NH4Cl + O2
D.NO2 + H2O
参考答案:C
本题解析:稀硝酸和铜反应,其还原产物是NO,氮气和氧气化合生成物是NO,氯化铵不能在氧气中反应,NO2溶于水是硝酸和NO,答案选C。
点评:该题是常识性知识的考查,难度不大。该题侧重对学生教材基础知识的巩固和训练,旨在巩固基础,提高能力。
本题难度:一般
2、计算题 一定量的铜与浓硝酸反应生成2.24 L NO2(标准状况下),求有多少克63%的浓硝酸中的溶质被还原。
参考答案:有10 g 63%的浓HNO3被还原。
本题解析:设质量为x的63%的浓HNO3中的溶质被还原为NO2
根据关系式计算:
HNO3?―? NO2
63 g? 22.4 L
x・63%? 2.24 L
得:63 g∶(x・63%)=22.4 L∶2.24 L
x="10" g
本题难度:简单
3、选择题 使用单质铜制取硝酸铜,最适宜的方法是: B
A.Cu+稀HNO3
B.Cu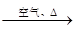 CuO
CuO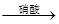 Cu(NO3)2
Cu(NO3)2
C.Cu+浓HNO3
D.Cu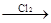 CuCl2
CuCl2 Cu(NO3)2
Cu(NO3)2
参考答案:B
本题解析:最适宜的方法是B ,因为不产生有毒的气体,对环境无污染。其他方法都有污染环境的地方。
本题难度:一般
4、选择题 标准状况下,在三个干燥的烧瓶内分别装入干燥纯净的NH3,含一半空气的氯化氢气体,NO2和O2按4∶1体积比混合的混合气体,然后分别做喷泉实验,三个烧瓶中所得溶液的物质的量浓度之比为
A.2∶1∶2
B.5∶5∶4
C.1∶1∶1
D.无法确定
参考答案:B
本题解析:
本题难度:一般
5、选择题 已知在某温度、101kPa的条件下3.01×1022个X气体分子的体积约为1.24L,则该条件下28g氮气的体积约为
A.22.4L/mol
B.24.8 L
C.2.48 L/mol
D.22.4 L
参考答案:B
本题解析:略
本题难度:一般