1、选择题 下列说法正确的是
A.含有离子键的化合物一定是离子化合物
B.含有共价键的化合物一定是共价化合物
C.所有物质都含有共价键
D.均由非金属元素形成的化合物不可能是离子化合物
参考答案:A
本题解析:含有离子键的化合物一定是离子化合物,全部由共价键形成的化合物是共价化合物,这说明在离子化合物中可能含有共价键,但在共价化合物中一定不可能含有离子键,因此选项A正确,B不正确。稀有气体单质分子中不存在化学键,C不正确;均由非金属元素形成的化合物要可能是离子化合物,例如氯化铵等铵盐,D不正确,答案选A。
点评:该题是中等难度的试题,也是高考中的常见题型和重要的考点。主要是考查学生对化学键含义以及化学键与化合物关系的熟悉了解程度,有利于培养学生规范的逻辑思维能力和灵活应变能力。该题的易错点是选项C。
本题难度:简单
2、填空题 (5分)能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。
(1))氢气在燃烧时,放出大量热量,说明该反应是 热反应,这是由于反应物的总能量 生成物的总能量(填“大于”、“小于”或“等于”,下同);从化学反应的本质角度来看,由于断裂反应物中的化学键吸收的总能量 形成产物的化学键放出的总能量
(2)氢气被公认为是21世纪代替矿物燃料的理想能源,5.2g氢气燃烧时放出286kJ热量,而每千克汽油燃烧时放出的热量为46000kJ。试据此分析氢气作为能源代替汽油的优势
。
参考答案:(1)放?大于?小于(各1分)
(2)清洁能源,燃烧后无污染环境的物质生成;单位质量放出的热量多。(2分)
本题解析:考查化学反应中的能量变化。
(1)如果反应物的总能量高于生成物的总能量,反应就是放热反应,反之是吸热反应。如果从化学变化的本质分析,在化学反应中断键是吸热的,形成化学键是放热,如果断键吸收的能量高于形成化学键所放出的能量,反应就是吸热反应,反之是放热反应。
(2)氢气的燃烧产物是水,没有污染。其次根据所给的数据分析,单位质量的氢气的放出的热量多于汽油放出的热量。
本题难度:一般
3、选择题
A.氯化铵
B.金刚石
C.冰醋酸
D.硫酸钠
参考答案:C
本题解析:冰醋酸在熔化时,只是克服分子间作用力,晶体结构没有被破坏。
本题难度:一般
4、选择题 下列图示内容的对应说明错误的是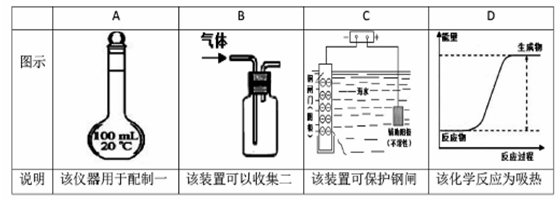
参考答案:A
本题解析:100ml容量瓶只能配制100ml的溶液,不能配制200毫升的溶液。故A错
考点:考查化学实验的相关知识点。
本题难度:一般
5、填空题 (8分)氯化溴(BrCl)的化学性质类似于卤素单质,试回答下列问题:
(1)氯化溴的电子式是?,它是由?键形成的?分子。
(2)氯化溴和水反应生成了一种三原子分子,该分子的电子式为?。
参考答案:(1)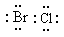 ;共价;共价;?(2)
;共价;共价;?(2)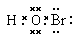
本题解析:(1)氯和溴都是非金属,形成的化学键是极性键,分子是极性分子,电子式为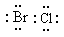 。
。
(2)氯化溴(BrCl)的化学性质类似于卤素单质,所以根据氯气和水反应的方程式可知,氯化溴和水反应生成物是氯化氢和次溴酸,因此次溴酸的电子式为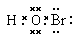 。
。
本题难度:一般