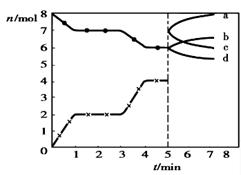
1��ѡ���� �����Ļ�ԭ��CO���ɽ�̿��CO2��Ӧ���á��ֽ���̿��CO2�������Ϊ2L���ܱ������У������½������з�Ӧ��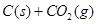

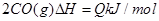 ����ͼΪCO2��CO�����ʵ���n��ʱ��t�ı仯��ϵͼ������˵����ȷ���ǣ�?��
����ͼΪCO2��CO�����ʵ���n��ʱ��t�ı仯��ϵͼ������˵����ȷ���ǣ�?��
A��0��1min��v��CO��=1mol/��L��min����1��3minʱ��
B���������ڵ�ѹǿ����ʱ����Ӧһ���ﵽƽ��״̬��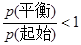
C��3minʱ�¶���T1���ߵ�T2��������ж�Q��0
D��5minʱ�ٳ���һ������CO��n��CO����n��CO2���ı仯�ɷֱ���a��b���߱�ʾ
�ο��𰸣�C
���������A������ʵĻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ������ڻ�ѧƽ��ʱҲ����ˣ����v��CO��=2v��CO2�����ʴ���B���ѧ��Ӧ��ʼ���ҽ��У����������ķ���ѹǿҲ���ʴﵽƽ��ʱ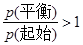 ���ʴ�����ѡC��
���ʴ�����ѡC��
�����������ص㿼����ǻ�ѧƽ������֪ʶ���е��Ѷȣ�����ѧ���Ի�ѧƽ��֪ʶ�����ճ̶Ⱥͼ���������
�����Ѷȣ���
2������� ��2 L�ܱ������ڣ�800 ��ʱ��Ӧ��2NO(g)+O2(g) 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯��� ��
��
ʱ��(s)
| 0
| 1
| 2
| 3
| 4
| 5
|
n(NO)(mol)
| 0.020
| 0.011
| 0.008
| 0.007
| 0.007
| 0.007
|
��1��д���÷�Ӧ��ƽ�ⳣ������ʽ��K=?��
��2����ͼ�б�ʾNO2�ı仯��������?����O2��ʾ��0~2s�ڸ÷�Ӧ��ƽ������v=?

��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����?��
a��v(NO2)=2v(O2)? b��������ѹǿ���ֲ���
c��v�� (NO)=2v��(O2)? d���������ܶȱ��ֲ���
��4��ijͬѧ�������ϵ�֪���÷�Ӧ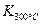 ��
�� ��25 ��ʱ������1 mol NO2�������仯Ϊ56.4 kJ�����Ǹ�ͬѧ�������������ע����+������-����������Ŀ��Ϣ���÷�Ӧ���Ȼ�ѧ����ʽΪ?��
��25 ��ʱ������1 mol NO2�������仯Ϊ56.4 kJ�����Ǹ�ͬѧ�������������ע����+������-����������Ŀ��Ϣ���÷�Ӧ���Ȼ�ѧ����ʽΪ?��
��5��Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����?��
a����ʱ�����NO2����? b���ʵ������¶�
c������O2��Ũ��? d��ѡ���Ч����
�ο��𰸣���12�֣���1��K=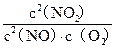 ?��2��b? 1.5��10-3mol��L��1��s��1?��3��b c?
?��2��b? 1.5��10-3mol��L��1��s��1?��3��b c?
��4�� 2NO(g)+O2(g) ?2NO2(g)? ��H=" -112.8" kJ ?��5��c
?2NO2(g)? ��H=" -112.8" kJ ?��5��c
�����������
�����Ѷȣ���
3��ѡ���� ij�����ܱ������У����淴ӦA(s) B + C(g) ��Q���ﵽƽ�⡣��С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ����·�����ȷ����
B + C(g) ��Q���ﵽƽ�⡣��С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ����·�����ȷ����
A������B��״ֻ̬��Ϊ��̬��Һ̬
B��ƽ��ʱ����λʱ����n(A)���ĩsn(C)����=1�s1
C������������䣬��ƽ����ϵ�м���B��ƽ��������淴Ӧ�����ƶ�
D������ʼʱ�������м���1molB��1molC���ﵽƽ��ʱ�ų�����Q
�ο��𰸣�C
���������A����С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ�˵��ƽ�������ƶ���B��״̬�������κ�״̬�����ԣ�����B��A������������У�C������Ҳ��ʾ������У������Ƿ�ƽ�⣬��������֮�ȶ���1:1������C������������䣬��� B����̬������B��ƽ����������ƶ�����ȷ��D������ʽ�����������1molB��1molC����������Q������ʼʱ�������м���1molB��1molC�������ǿ��淴Ӧ����������ȫ���е��ף��ų�����С��Q������
�����Ѷȣ�һ��
4��ѡ���� ���³�ѹ�£�ע��������װ��NO2���壬ע��������װ����ͬ����Ŀ�����ע������U �ι���ͨ����ͼ��ʾ��������ֹˮ�У�ͬʱ��������ע�����Ļ������������ľ�����ȣ����ῴ��U�ι���Һ��(�����Ǵ�������NO2��ˮ�ķ�Ӧ)��?��

A��a��������b���½�
B��a���½���b������
C��U�ι���Һ���ޱ仯
D�����ж�
�ο��𰸣�B
�������������������ʱ��ƽ��2NO2=N2O4�����ƶ���ʹ��������ѹǿ������������ѹǿ�����a���½���b������������B��ȷ��
�����Ѷȣ�һ��
5��ѡ���� 2��0mol PCl3��1��0mol Cl2�������������ܱ������У���һ�������·���������Ӧ��
PCl3(g)��Cl2(g)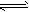 PCl5(g)��ƽ��ʱ��PCl5Ϊ0��40mol�������ʱ����1��0mol PCl3��0��50mol Cl2������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ�����
PCl5(g)��ƽ��ʱ��PCl5Ϊ0��40mol�������ʱ����1��0mol PCl3��0��50mol Cl2������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ�����
[? ]
A��0��40mol
B��0��20mol
C����0��20mol
D������0��20mol����0��40mol
�ο��𰸣�C
���������
�����Ѷȣ�һ��