1、选择题 最近,兰州近代物理研究所研制出我国首批氧-18气体。氧-18是氧的一种同位素,称为重氧,下列说法正确的是
[? ]
A.1.8g氧-18气体的物质的量是0.1mol
B.0.1mol重氧气体的体积是2.24L
C.重氧气体的摩尔质量为36g
D.0.1mol重氧水所含中子数约是6.02×1023个
参考答案:D
本题解析:
本题难度:简单
2、填空题 实验室用Na2CO3·10H2O晶体配制0.02 mol/L的Na2CO3溶液480 mL。
(1)① 实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少 ;
② 实验中两次用到玻璃棒,其作用分别是 、 。
(2) 应用托盘天平称取Na2CO3·10H2O晶体的质量为: g。
(3)根据下列操作对所配溶液的浓度各有什么影响,将其序号填在下面空格:
①碳酸钠晶体失去了部分结晶水; ②用“左码右物”的称量方法称量晶体;
③碳酸钠晶体不纯,其中混有氯化钠; ④容量瓶中原有少量蒸馏水。
⑤定容时俯视液面;⑥摇匀后发现液面低于刻度线再加水。
其中引起所配溶液浓度:a.偏高的有 ;
b.偏低的有 ;
c.无影响的有 。
参考答案:(1)①500 mL容量瓶(1分)、胶头滴管(1分) ② 搅拌,加快固体溶解(1分) 引流(1分)
(2)2.9 (2分) (3)a.①⑤ b.②③⑥ c. ④(每个序号1分)
本题解析:(1)根据操作步骤选取实验仪器;配制步骤有计算、称量、溶解、移液、洗涤、定容、摇匀等操作,固体药品一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,并用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,① 实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少500 mL容量瓶、胶头滴管;② 实验中两次用到玻璃棒,其作用分别是搅拌,加快固体溶解、 引流。
(2)m=nM=CVM=0.02mol/L×0.5L×286g/mol=2.9g。
(3)①碳酸钠晶体失去了部分结晶水,导致称量溶质碳酸钠的质量增大,配制溶液的浓度偏高;②用“左码右物”的称量方法称量晶体导致称量溶质的质量增小,配制溶液的浓度偏低;③碳酸钠晶体不纯,其中混有氯化钠,导致碳酸钠的物质的量偏小,配制溶液的浓度偏低;④容量瓶未经干燥就使用不影响溶质的物质的量,也不影响溶液的体积,所以对配制的溶液浓度无影响;⑤定容时俯视液面,所配溶液的体积偏小,浓度偏高;⑥摇匀后发现液面低于刻度线再加水,所配溶液的体积偏大,浓度偏低;综上所述,偏高的为:①⑤,偏低的为:②③⑥,无影响的为:④。
考点:考查一定物质的量浓度溶液的配制。
本题难度:一般
3、选择题 向等体积等物质的量浓度的NaCl、MgCl2两溶液中分别滴加等浓度的AgNO3溶液使Cl-恰好沉淀完全,则消耗AgNO3溶液的体积之比为
A.1:1
B.1:2
C.2:1
D.1:3
参考答案:B
本题解析:分析:等体积、等物质的量浓度的NaCl、MgCl2两种溶液中溶质的物质的量相等,分别与等物质的量浓度的AgNO3溶液恰好完全反应,则消耗的硝酸银的物质的量之比等于它们的体积比.
解答:设等体积、等物质的量浓度的NaCl、MgCl2溶液中溶质的物质的量均为1mol,
则与等物质的量浓度的AgNO3溶液恰好完全反应时存在:
1molNaCl~1molAgNO3,
1molMgCl2~2molAgNO3,
由n=cV可知,物质的量之比等于溶液的体积之比,
所以与NaCl、MgCl2两种溶液反应的AgNO3溶液的体积比为1:2,
故选B.
点评:本题考查物质的量浓度的计算,明确物质的量、浓度及物质的构成的关系,氯离子与银离子的反应是解答本题的关键,难度不大.
本题难度:简单
4、选择题 铅笔芯的主要成分是石墨和粘土,这些物质按照不同的比例加以混和、压制,就可以制成铅笔芯。如果铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为1mg。那么一个铅笔字含有的碳原子数约为
[? ]
A.2.5×1019个
B.2.5×1022个
C.5×1019个
D.5×1022个
参考答案:A
本题解析:
本题难度:简单
5、选择题 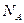 代表阿伏加德罗常数,下列说法正确的是(? )
代表阿伏加德罗常数,下列说法正确的是(? )
A.2.3 g钠由原子变成离子时,失去的电子数为0.1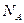
B.0.2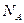 个硫酸分子与19.6 g磷酸含有相同的氧原子数
个硫酸分子与19.6 g磷酸含有相同的氧原子数
C.28 g氮气所含的原子数为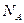
D.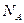 个氧分子与
个氧分子与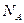 个氢分子的质量比为8∶1
个氢分子的质量比为8∶1
参考答案:AB
本题解析:本题体现的是以摩尔为中心的计算,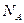 与摩尔的关系并由此延伸到粒子个数、物质的质量,应熟练掌握它们的换算关系。
与摩尔的关系并由此延伸到粒子个数、物质的质量,应熟练掌握它们的换算关系。
A选项中钠为+1价,2.3 g钠为0.1 mol钠原子,失去电子数为0.1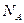 。正确。
。正确。
B选项中19.6 g磷酸即为0.2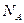 个磷酸分子(19.6 g÷98 g・mol
个磷酸分子(19.6 g÷98 g・mol ="0.2" mol),等物质的量的硫酸(H2SO4)与磷酸(H3PO4)含有相同的氧原子数。正确。
="0.2" mol),等物质的量的硫酸(H2SO4)与磷酸(H3PO4)含有相同的氧原子数。正确。
C选项中28 g氮气(N2)即为1摩氮分子(28 g÷28 g・mol ="1" mol),所以含2
="1" mol),所以含2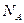 个氮原子,错误。
个氮原子,错误。
D选项中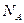 个氧分子质量为32 g,
个氧分子质量为32 g,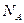 个氢分子质量为2 g,则其质量比为16∶1。错误。
个氢分子质量为2 g,则其质量比为16∶1。错误。
本题难度:简单