1、选择题 二次世界大战时,科学家玻尔为避免诺贝尔奖章落入德军手中,将金质奖章溶解在“王水”中,其化学方程式:Au+HNO3+4HCl=HAuCl4+x↑+2H2O,则x的化学式为( )
A.NO
B.NO2
C.N2O
D.NH3
参考答案:A
本题解析:
本题难度:简单
2、填空题 Ⅰ.用MnO2氧化密度为1.19 g・cm-3,溶质质量分数为36.5%的HCl溶液。反应的化学方程式为:
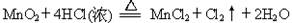
(1)该盐酸的物质的量浓度为 mol/L。
(2)用双线桥法表示出该反应的电子转移方向和数目 。
(3)8.7gMnO2能使 molHCl被氧化。
Ⅱ.在一定体积的18 mol/L的浓硫酸中加入过量铜片,加热使之反应,若被还原
的硫酸为 0.9 mol。则浓硫酸的实际体积_________(填“大于”、“等于”或“小于”)100mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为________________________________________________。
参考答案:Ⅰ(1)11.9
(2)
(3)0.2
Ⅱ 大于 3Cu+8H++2NO3-=3Cu2++2NO +4H2O
本题解析:Ⅰ.(1)有公式c="1000pw/M=1000×1.19×36.5%/36.5=11.9" mol/L;
(2)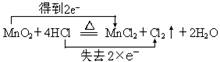
(3)在反应中MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
1mol MnO2氧化2mol浓盐酸,所以8.7gMnO2能使0.2molHCl被氧化.
Ⅱ.已知反应 Cu+2H2SO4 CuSO4+2H2O+SO2 ↑硫酸有一半被还原所以硫酸总物质的量为2×0.9="1.8(mol)"
CuSO4+2H2O+SO2 ↑硫酸有一半被还原所以硫酸总物质的量为2×0.9="1.8(mol)"
又知,硫酸的物质的量浓度为18mol/L ;所以原体积为1.8/18=0.1L;参加反应H2SO4为0.9mol×2=1.8mol,体积100mL,因反应后稀H2SO4不与Cu反应,故H2SO4体积应大于100mL。加入硝酸盐后,相当于铜与稀硝酸反应,3Cu+8H++2NO3-=3Cu2++2NO +4H2O
考点:实验室制取氯气的反应,及铜与浓硫酸的反应
本题难度:一般
3、选择题 某溶液中有Fe2+、Cl-和I-共存,要氧化除去I-而不影响Fe2+和Cl-,可加入的试剂是(?)
A.Cl2
B.KMnO4
C.FeCl3
D.HCl
参考答案:C
本题解析:分析各选项知,D中HCl无氧化性;A中的Cl2和B中KMnO4能氧化Fe2+和I-。
本题难度:一般
4、选择题 在5ml0.05mol/L的某金属氯化物的溶液中,滴加
0.1mol/LAgNO3溶液,生成沉淀的质量与加入AgNO3溶液的体积关系如图所示,则该氯化物中金属元素的化合价为
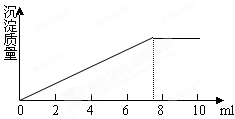
A.+1
B.+2
C.+3
D.+4
参考答案:C
本题解析:
分析:根据氯离子和银离子之间反应生成氯化银沉淀的实质以及氯化物的化学式进行计算.
解答:解:氯化物种的Cl-和Ag+1:1反应,因此消耗掉的硝酸银的物质的量为这些溶液中Cl-离子的物质的量,n(Cl-)=n(Ag+)=7.5×10-3L×0.1mol/L=7.5×10-4mol.
设该金属的化合价为X其化学式为A(Cl)x,n(Ax+)=5×10-3L×0.05mol/L=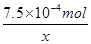 ,解得x=3.
,解得x=3.
故选C.
点评:本题考查学生分析和解决问题的能力,是一道有关离子反应的计算题,难度不大.
本题难度:简单
5、选择题 下列物质久置于空气中会发生相应的变化,其中发生了氧化还原反应的是
[? ]
A.浓盐酸挥发
B.澄清的石灰水变浑浊
C.氢氧化钠溶液久置于空气中
D.铁在潮湿的空气中生锈
参考答案:D
本题解析:
本题难度:简单