1、填空题 (9分)下图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性,请根据图示回答下列问题:
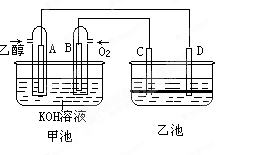
(1)通入乙醇(C2H5OH)的惰性电极的电极反应式为 。
若甲池可以充电,充电时A接电源的负极,此时B极发生的电极反应式为 。
(2)在乙池反应过程中,可以观察到 电极周围的溶液呈现棕褐色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色,C极发生的电极反应 。
(3)若在常温常压下,1gC2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,表示该反应的热化学方程式为 。
2、选择题 某同学按下图所示的装置进行实验.?A?、?B?为两种常见金属,它们的硫酸盐可溶于水.当?K?闭合时,在交换膜处?SO42-从右向左移动.下列分析正确的是?
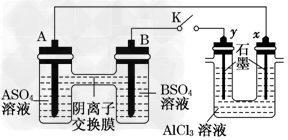
[? ]
A.溶液中A2+浓度减小
B.B?的电极反应:?B-2e-===B2+?
C.y电极上有H2产生,发生还原反应
D.反应初期,?x电极周围出现白色胶状沉淀,不久沉淀溶解
3、实验题 二氧化氯(ClO2)为一种黄绿色气体,是一种高效、广谱、安全的杀菌、消毒剂。制备ClO2的方法有多种。
(1)纤维素还原法制ClO2。其原理是:纤维素水解得到的最终产物A与NaClO3反应生成ClO2。完成反应的化学方程式:其流程如下:□(A)+□NaClO3+□H2SO4=□ClO2↑+□CO2↑+□H2O+□______
(2)电解食盐水制取ClO2 ,其流程如下:
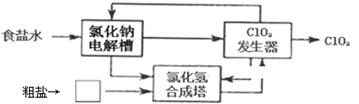
①粗盐中含有Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中加入试剂的顺序依次为__________(填化学式),充分反应后将沉淀一并滤去,再加入盐酸。
②食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸在发生器中反应生成ClO2 ,写出发生器中生成ClO2的化学方程式____________________。
③上述流程中,可循环利用的物质有__________;按照绿色化学原则,电解槽阴极产生的气体与方框中物质的物质的量之比为________时,原子的利用率为100%。
(3)实验室以NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程下如下:

已知:(I)A气体在标准状况下的密度为0.089g/L;
(Ⅱ)气体B能使湿润的红色石蕊试纸变蓝。
①电解时,发生反应的化学方程式为 。
②NCl3与NaClO2(亚氯酸钠)按物质的量之比为1∶6混合,在溶液中恰好反应生成ClO2,该反应的离子方程式为 。
4、填空题 铝合金以质轻、稳定性好等优点广泛应用于航空航天事业。在铝合金表面能形成一层较厚的氧化膜,这是其在空气中稳定存在的关键。其反应原理是以铝件与另一种材料为电极,以某种溶液作电解质溶液进行电解,通电后在铝件与电解质溶液的接触面上逐渐形成一层氢氧化铝薄膜,薄膜的某些部位存在着小孔,电流从小孔中通过并产生热量使氢氧化铝分解,从而使铝件表面形成一层较厚的氧化膜。某校课外兴趣小组的同学根据上述原理,以铝件和铁棒为电极,以一定浓度的碳酸氢钠溶液为电解质溶液进行实验,实验装置如图所示
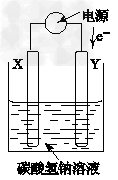
(1)铝件放在________(填“X”或“Y”)极。
(2)铝件表面形成氢氧化铝的电极反应式是_____________________________。
(3)电解过程中,必须使电解质溶液的pH保持相对稳定(不能太大也不能太小)的原因是____________________________。
(4)用碳酸氢钠溶液作电解质溶液,而不用碳酸钠溶液作电解质溶液,其理由是_____________________________________。
5、选择题 以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Au等杂质)的电解精炼,下列说法正确的是
A.利用阳极泥可回收Ag、Au等金属
B.阳极减少的质量一定等于阴极增加的质量
C.精炼过程中,CuSO4溶液的浓度不发生改变
D.因部分电能转化为热能,精炼时通过的电量与阴极铜的析出量无确定关系