| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《水的电离平衡》练习题(八)
参考答案:C 本题解析: A、取NaOH溶液时仰视读数,会使氢氧化钠的体积偏多,造成消耗盐酸的体积偏多,测定结果偏高,错误;B、滴定结束后,滴定管尖嘴处有一悬挂液滴,对结果无影响,错误;C、锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度,会造成假滴定 终点的判断,使消耗盐酸的体积偏少,测定结果偏低,正确;D、盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2次~3次,会使氢氧化钠的体积偏多,造成消耗盐酸的体积偏多,测定结果偏高,错误,答案选C。 本题难度:一般 3、选择题 常温下c(H+)最小的是( ) |
参考答案:C
本题解析:pH=0的溶液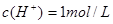 ;0.03 mol・L-1 H2SO4溶液
;0.03 mol・L-1 H2SO4溶液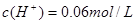 ;0.05 mol・L-1 HClO溶液中因HCLO为弱酸,所以
;0.05 mol・L-1 HClO溶液中因HCLO为弱酸,所以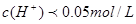 ;0.05 mol・L-1的NaHSO4溶液
;0.05 mol・L-1的NaHSO4溶液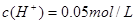
本题难度:一般
4、简答题 室温时,等物质的量浓度的四种溶液:①HClO ②NaCl ③HCl ④NaOH中,水的电离程度是否相同?为什么?
参考答案:不同;当物质的量浓度相同时,HCl溶液中的c(H+)与NaOH溶液中的c(OH-)相同,对水的电离平衡的抑制程度相同,故这两种溶液中水的电离程度相同。NH4Cl溶液中,NH4+与OH-结合,c(OH-)降低,平衡正向移动,水的电离程度增大。在NaCl溶液中,Na+与Cl-均不能与水电离的H+、OH-结合形成弱电解质,故水的电离平衡不发生变化。所以,这四种溶液中水的电离程度不同,按水的电离程度由大到小的顺序为:①>②>③=④。
本题解析:
本题难度:一般
5、选择题 设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,8 g甲烷中含C-H键的数目为4NA
B.25℃时,1 L pH=13的Ba(OH) 2溶液中含有的OH―数为0.2NA
C.1 mol冰醋酸和1 mol乙醇经催化加热反应生成H2O分子数为NA
D.标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移的电子总数为0.1NA
参考答案:D
本题解析:A、CH4分子含有4个C―H键,8g甲烷物质的量为8g÷16g/mol=0.5mol,所以8 g甲烷中含C-H键的数目为2NA,故A错误;B、pH=13的Ba(OH) 2溶液OH?浓度为:0.1mol?L?1,所以1 L pH=13的Ba(OH) 2溶液中含有的OH―数为0.1NA,故B错误;C、醋酸与乙醇发生的酯化反应是可逆反应,所以1 mol冰醋酸和1 mol乙醇经催化加热反应生成H2O分子数小于NA,故C错误;D、Cl2与稀NaOH溶液反应时,物质的量对应关系为:Cl2~e?,2.24LCl2物质的量为1mol,与稀NaOH溶液反应,转移的电子总数为0.1NA,故D正确。
考点:本题考查阿伏加德罗常数的计算。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点归纳《食品添加剂.. | |