|
高考化学知识点总结《水的电离平衡》练习题(十)
2020-08-23 06:55:18
【 大 中 小】
|
1、选择题 电解质溶液中,阴离子和阳离子均以水合离子形式存在,如H+可以结合一个水分子形成H3O+.下列物质的电离方程式错误的是( )
A.CuSO4═Cu2++SO42-
B.HCl+H2O═H3O++Cl-
C.NaHCO3═Na++HCO3-
D.NaHSO4═Na++HSO4-
参考答案:D
本题解析:
本题难度:简单
2、选择题 &nb sp;把1 mL 0.1 mol/L的H2SO4加水稀释成2 L溶液,在此溶液中由水电离产生的H+,其浓度接近于
A.1×10-4 mol/L
B.1×10-8 mol/L
C.1×10-11 mol/L
D.1×10-10 mol/L
|
参考答案:D
本题解析:稀释后硫酸的浓度为5×10—5mol/l,氢离子浓度为10—4mol/l,则溶液中的c(OH—)=10—10mol/l。
而酸溶液中,OH—全部来自于水的电离,故由水电离出的c(H+)=10—10mol/l,答案为D
本题难度:一般
3、填空题 已知水在25℃和95℃时,其电离平衡曲线如右图所示:
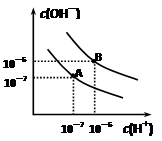
⑴则25 时水的电离平衡曲线应为 (填“A”或“B”)。 时水的电离平衡曲线应为 (填“A”或“B”)。
⑵25 时,将 时,将 =8的NaOH溶液与 =8的NaOH溶液与 =5的 =5的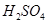 溶液混合,若所得混合溶液的 溶液混合,若所得混合溶液的 =7,则NaOH溶液与 =7,则NaOH溶液与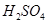 溶液的体积比为 。 溶液的体积比为 。
⑶95 时,0.1 mol/L的NaOH溶液的pH值是 。 时,0.1 mol/L的NaOH溶液的pH值是 。
⑷95 时,若100体积 时,若100体积 1= 1=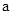 的某强酸溶液与1体积 的某强酸溶液与1体积 2=b的某强碱溶液混合后溶液呈中性,则混合前, 2=b的某强碱溶液混合后溶液呈中性,则混合前,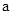 与b之间应满足的关系是 与b之间应满足的关系是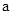 = (用含b的代数式表示),a+b_______14(填“<”、“=”或“>”)。 = (用含b的代数式表示),a+b_______14(填“<”、“=”或“>”)。
参考答案:⑴A ⑵10:1 ⑶11 ⑷14-b,=
本题解析:(1)电离是吸热,则升高温度,电离程度增加,水中氢离子浓度增加,所以25 ℃时水的电离平衡曲线应为A。
(2)若所得混合溶液的pH=7,则 ,解得 ,解得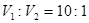 。 。
(3)95 时,0.1 mol/L的NaOH溶液中OH-的浓度是0.1mol/L,则溶液中氢离子的浓度是10-11mol/L,则溶液的pH值是11。 时,0.1 mol/L的NaOH溶液中OH-的浓度是0.1mol/L,则溶液中氢离子的浓度是10-11mol/L,则溶液的pH值是11。
(4)95℃时若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则 ,所以该强酸的pH1与强碱的pH2之间应满足的关系是a+b=14。 ,所以该强酸的pH1与强碱的pH2之间应满足的关系是a+b=14。
考点:考查外界条件对水的电离平衡的影响、pH的计算
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生基础知识的巩固与训练,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是明确随着温度的升高,水的离子积常数是增大,在计算pH时需要灵活运用。
本题难度:一般
4、实验题 (12分)酸碱中和滴定是中学化学中重要的定量实验之一。
Ⅰ.某研究性学习小组准确进行了如下实验,称取1.00g不纯的苛性钠样品配成250ml溶液,取出10.00ml,用已知浓度为0.040mol·L-1的盐酸进行滴定(杂质不与盐酸反应)。
根据要求回答下列问题:
(1)配制250 mL 0.040mol·L-1的盐酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、___________和______________。
(2)为测定该苛性钠溶液的准确浓度,几次滴定消耗盐酸的体积如下:
实验序号
| 1
| 2
| 3
| 4
| 消耗盐酸溶液的体积(mL)
| 20.05
| 20.00
| 22.10
| 19.95
|
①计算苛性钠浓度时,哪次实验的数据不宜采用?答:________。(填实验序号)
②该苛性钠溶液的浓度为___________。
(3)若操作过程中未用盐酸润洗滴定管,对测定结果有怎样的影响?
答:______________________(填“偏大”、“偏小”或“无影响”)。
Ⅱ.在另一次实验中,研究性小组将V1 mL 1.0mol·L-1 HCl溶液和V2 mL 未知浓度的NaOH溶液均匀混合后,测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2="50" mL)。

(4)下列叙述中正确的是_________
A.该实验的环境温度为22℃
B.当V1 =40时,溶液中c(Na+)<c(Cl—)
C.NaOH溶液的浓度为1.0mol·L-1
D.保持其他条件不变,只将HCl改为CH3COOH进行实验,也得到如图的实验结果
参考答案:(Ⅰ)(1)250ml容量瓶胶头滴管(写“容量瓶”不给分)
(2)①3②0.080mol·L-1(3)偏大
(Ⅱ)(4)B
本题解析:(Ⅰ)(1)配制250毫升溶液必须使用250ml容量瓶,定容时需要使用胶头滴管。(2)①实验3的数据和其他数据差距较大,所以不宜采用。②所用的盐酸的平均体积为20.00毫升,所以氢氧化钠的浓度为20.00×0.040mol·L-1/10.00=0.080mol·L-1。(3)若未用盐酸润洗滴定管,则盐酸的浓度偏小,用的体积偏大,则结果偏大。(Ⅱ)(4)A、图像表示的酸碱中和后的温度,所以不能说明环境温度为22℃;B、从图像分析,当盐酸的体积为30毫升时,溶液的温度最高,说明酸碱恰好完全反应,所以当盐酸的体积为40时,溶液中的钠离子浓度小于氯离子浓度;C、根据盐酸体积为30毫升进行计算,氢氧化钠的浓度=1.0×30/(50-30)=1.5mol/L;D、醋酸为弱酸,不能完全电离,所以反应放出热量少。所以选B。
考点:溶液的配制和酸碱中和滴定。
本题难度:困难
5、填空题 (12分)(1)25℃时,浓度为0.1 mol·L-1的6种溶液:
①HCl, ②CH3OOH, ③Ba(OH)2,④Na 2CO3,⑤KCl,⑥NH4Cl溶液
pH由小到大的顺序为_________________ _(填写编号)。
(2)25℃时,醋酸的电离常数Ka=1.7×10-5mol/L,则该温度下CH3COONa的水解平衡常数
Kh= mol ·L-1(保留到小数点后一位)。
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈 (填“酸性”,“中性”或“碱性”),请写出离子浓度大小关系式: 。
(4)25℃时,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后,溶液的pH=7,则溶液中c(CH3COO-)+ c(CH3COOH)= ,m与n的大小关系是m n(填“>”“=”或“<”)。
参考答案:(1)①②⑥⑤④③ (2) 5.9×10-10 (3) 酸性 c(CH3COO-)>c(Na+)>c(H+)>c(OH-)。(4) m/2 mol/L >
本题解析:(1)①HCl是一元强酸, ②CH3OOH是一元弱酸, ③Ba(OH)2是二元强碱,④Na 2CO3是强碱弱酸盐,⑤KCl是强酸强碱盐,⑥NH4Cl是强酸弱碱盐。酸性:强酸大于弱酸大于强酸弱碱盐;碱性:碱的大于强碱弱酸盐的。所以这几种溶液pH由小到大的顺序为①②⑥⑤④③.
(2)KHAc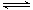 CH3COO-+H+, CH3COO-+H+, ,该温度下CH3COONa的水解平衡为CH3COO-+H2O ,该温度下CH3COONa的水解平衡为CH3COO-+H2O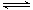 CH3COOH+OH-。 CH3COOH+OH-。
水解平衡常数  
所以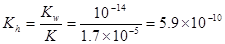 。(3)25℃时,pH=3的醋酸,c(H+)=10-3mol/L, pH=11的氢氧化钠溶液,c(H+)=10-11mol/L,则c(OH-)=Kw÷c(H+)=10-14÷10-11=10-3mol/L.两种溶液中的离子浓度相等。当等体积混合后,电离的部分巧合完全中和。但由于醋酸为弱酸。还有大量为电离的醋酸分子存在,会继续电离产生H+和CH3COO-。所以溶液呈酸性。在溶液中存在电荷守恒。c(Na+) + c(H+) = c(CH3COO-) + c(OH-)。(4)由于溶液为等体积混合,所以溶液中c(CH3COO-) + c(CH3COOH)=m/2mol/L。因为酸是弱酸,碱是强碱,若等物质的量混合,这恰好生成CH3COONa。溶液由于CH3COO-的水解二显碱性。为了使溶液显中性,酸必须稍微过量一些,来抵消醋酸根离子水解的碱性。所以m与n的大小关系是m>n. (5)25℃时,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7 ,说明醋酸与一水合氨的强弱程度相同。也就是电离程度相等。由于醋酸的电离平衡常数为Ka=1.7×10-5mol/L所以NH3·H2O的电离常数Ka=1.7×10-5mol/L。 。(3)25℃时,pH=3的醋酸,c(H+)=10-3mol/L, pH=11的氢氧化钠溶液,c(H+)=10-11mol/L,则c(OH-)=Kw÷c(H+)=10-14÷10-11=10-3mol/L.两种溶液中的离子浓度相等。当等体积混合后,电离的部分巧合完全中和。但由于醋酸为弱酸。还有大量为电离的醋酸分子存在,会继续电离产生H+和CH3COO-。所以溶液呈酸性。在溶液中存在电荷守恒。c(Na+) + c(H+) = c(CH3COO-) + c(OH-)。(4)由于溶液为等体积混合,所以溶液中c(CH3COO-) + c(CH3COOH)=m/2mol/L。因为酸是弱酸,碱是强碱,若等物质的量混合,这恰好生成CH3COONa。溶液由于CH3COO-的水解二显碱性。为了使溶液显中性,酸必须稍微过量一些,来抵消醋酸根离子水解的碱性。所以m与n的大小关系是m>n. (5)25℃时,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7 ,说明醋酸与一水合氨的强弱程度相同。也就是电离程度相等。由于醋酸的电离平衡常数为Ka=1.7×10-5mol/L所以NH3·H2O的电离常数Ka=1.7×10-5mol/L。
考点:考查离子浓度的大小比较、电离平衡常数与盐的水解平衡常数的关系、溶液的酸碱性
本题难度:困难
| 