1、填空题 过氧化钙(CaO2)难溶于水,在常温下稳定,在潮湿空气及水中缓慢分解放出氧气,因而广泛应用于渔业、农业、环保等许多方面。下图是以大理石(主要杂质是氧化铁)等为原料制取过氧化钙(CaO2)的流程。
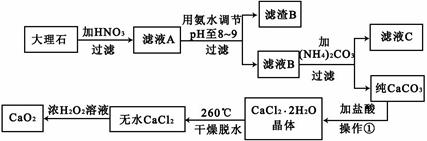
请回答下列问题:
(1)用氨水调节pH至8――9的目的是?。
(2)若测得滤液C中c(CO32-)=10-3mol/L,则Ca2+?(填“是”或“否”)沉淀完全。(已知c(Ca2+)≤10-5mol/L可视为沉淀完全;Ksp(CaCO3)=4.96×10-9)
(3)若在滤液C中,加入HNO3使溶液呈酸性以得到副产物NH4NO3,则酸化后溶液中,c(NH4+) ?c(NO3-)(填“≥”、“≤”、“<”、“>”或“=”)。
(4)在低温下,往过氧化氢浓溶液中投入无水氯化钙进行反应,写出该反应的化学方程式:?,一段时间后,再加入氢氧化钠溶液,当调节溶液pH至9――11,才出现大量沉淀。用化学方程式和简要的文字解释需用氢氧化钠调节pH至9――11的原因?。
2、填空题 下图是工业上生产碳酸锂的部分工艺流程,请根据流程图及已知信息回答问题。
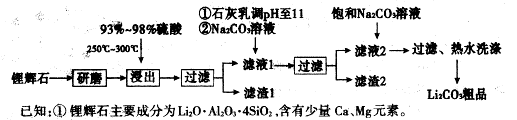
②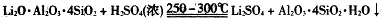
③几种物质不同温度下的溶解度。
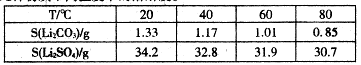
(1)从滤渣1中分离出Al2O3的部分流程如下图所示,括号表示加入的试剂,方框表示所得到的物质。写出图中①、②、③表示的各物质,步骤II中反应的离子方程式是?。
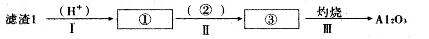
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3,写出生成滤渣2反应的离子方程式:
?。
(3)向滤液2中加入饱和Na2CO,溶液,过滤后,用“热水洗涤”的原因是?。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下。
①将粗产品Li2CO3溶于盐酸作用解槽的阳极液,LiOH溶液作阴极液,两者用离子选择半透膜隔开,用惰性电极电解。阳极的电极反应式是?。
②电解后向产品LiOH溶液中加入过量NH4HCO,溶液生成Li2CO3反应的化学方程式是?。
3、选择题 金属的冶炼有三种方法,那么冶炼银、铁、铝分别应采用
A.热分解法、热还原法、电解法
B.热还原法、热分解法、电解法
C.电解法、热还原法、热分解法
D.电解法、热分解法、热还原法
4、选择题 北京2008年奥运会金牌“金镶玉”环形玉壁由昆仑玉制成,昆仑玉的成分可简单看成是Ca2Mg5Si8O22(OH)2,则其用二氧化硅和金属氧化物的形式可表示为( ? )
A.CaO?MgO?SiO2?H2O
B.2CaO?5MgO?8SiO2?H2O
C.2CaO?MgO?SiO2?2H2O
D.5CaO?2MgO?8SiO2?H2O
5、填空题 工业上用黄铜矿冶炼铜及对炉渣综合利用的一种工艺流程如下:
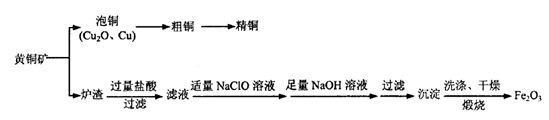
(1)冶炼过程中得到Cu2O和Cu的混合物称为“泡铜”,其与金属A1在高温条件下混合反应可得粗铜,反应化学方程式为________。粗铜精炼时应将粗铜连接在直流电源的____极,可在____极得到纯度较高的精铜。
(2)传统炼铜的方法主要是火法炼铜,其主要反应为:
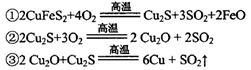
每生成1 mol Cu,共消耗____mol O2。反应③中的氧化剂是____。
(3)炼铜产生的炉渣(含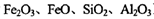 )可制备Fe2O3。根据流程回答下列问题:
)可制备Fe2O3。根据流程回答下列问题:
①加入适量NaClO溶液的目的是_______ (用离子方程式表示)。
②除去Al3+的离子方程式是____。
③选用提供的试剂,设计实验验证炉渣中含有FeO。提供的试剂有:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水。所选试剂是____。实验设计:________。